题目内容
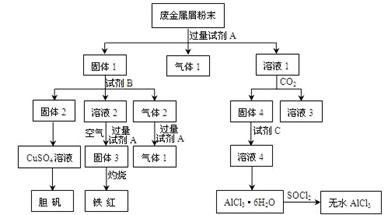
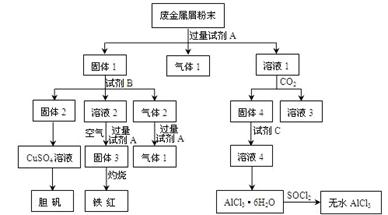
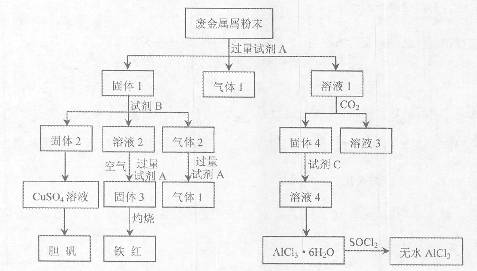
某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4?5H2O)、无水AlCl3和铁红的过程如图所示:

已知:①Al3+、Al(OH)3、AlO2-有如下转化关系:Al3+
Al(OH)3
AlO2-
②碳酸不能溶解Al(OH)3.
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是
(2)溶液2中含有的金属阳离子是
(3)溶液2转化为固体3的反应的离子方程式是
(4)固体2制取CuSO4溶液有多种方法.
①在固体2中加入浓H2SO4,并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是
②在固体2中加入稀H2SO4 后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是
(6)直接加热AlCl3?6H2O不能得到无水AlCl3.SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体.AlCl3?6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是

已知:①Al3+、Al(OH)3、AlO2-有如下转化关系:Al3+
| OH- |
| H+ |
| OH- |
| H+ |
②碳酸不能溶解Al(OH)3.
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是
2Al+2OH-+2H2O=2 AlO2-+3H2↑
2Al+2OH-+2H2O=2 AlO2-+3H2↑
.(2)溶液2中含有的金属阳离子是
Fe2+
Fe2+
;气体2的成分是CO2和H2
CO2和H2
.(3)溶液2转化为固体3的反应的离子方程式是
4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓
4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓
.(4)固体2制取CuSO4溶液有多种方法.
①在固体2中加入浓H2SO4,并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
②在固体2中加入稀H2SO4 后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是
2Cu+4H++O2
2Cu2++2H2O
| ||
2Cu+4H++O2
2Cu2++2H2O
.
| ||
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是
若在溶液1中直接加入盐酸,会使溶液4中混有试剂A中的阳离子(如Na+等),而不是纯净的AlCl3溶液
若在溶液1中直接加入盐酸,会使溶液4中混有试剂A中的阳离子(如Na+等),而不是纯净的AlCl3溶液
.(6)直接加热AlCl3?6H2O不能得到无水AlCl3.SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体.AlCl3?6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是
AlCl3?6H2O+6SOCl2
AlCl3+12HCl↑+6SO2↑
| ||
AlCl3?6H2O+6SOCl2
AlCl3+12HCl↑+6SO2↑
.
| ||
分析:(1)根据转化图可知,固体1最终生成胆矾和铁红,这说明固体1中含有铁和铜两种元素.所以试剂A应该是氢氧化钠溶液,则气体是铝和氢氧化钠反应生成的氢气;
(2)固体2最终得到胆矾,这说明固体2是铜,则试剂B不应该是碱液.根据气体2和氢氧化钠溶液反应又有气体1产生,这说明试剂B应该是硫酸,气体2中含有CO2和氢气,而溶液2中含有亚铁离子.
(3)固体3灼烧生成铁红,所以固体3是氢氧化铁,则溶液2转化为固体3的反应的离子方程式是4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓.
(4)铜和稀硫酸不反应,但氧气能氧化单质铜生成氧化铜,进而生成硫酸铜,反应的方程式是2Cu+4H++O2=Cu2++2H2O.
(5)溶液1中含有偏铝酸钠,试剂C是盐酸.如果向溶液1中+加试剂C→溶液4”,则溶液4中将混有试剂A中的阳离子(如Na+等),而使AlCl3溶液不纯净.
(6)氯化铝水解,所以直接加热得不到氯化铝,需要在氯化氢的气氛中加热.SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体,所以根据原子守恒可知,该气体应该是二氧化氯,则反应的方程式是AlCl3?6H2O+6SOCl2=AlCl3+12HCl+6SO2↑.
(2)固体2最终得到胆矾,这说明固体2是铜,则试剂B不应该是碱液.根据气体2和氢氧化钠溶液反应又有气体1产生,这说明试剂B应该是硫酸,气体2中含有CO2和氢气,而溶液2中含有亚铁离子.
(3)固体3灼烧生成铁红,所以固体3是氢氧化铁,则溶液2转化为固体3的反应的离子方程式是4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓.
(4)铜和稀硫酸不反应,但氧气能氧化单质铜生成氧化铜,进而生成硫酸铜,反应的方程式是2Cu+4H++O2=Cu2++2H2O.
(5)溶液1中含有偏铝酸钠,试剂C是盐酸.如果向溶液1中+加试剂C→溶液4”,则溶液4中将混有试剂A中的阳离子(如Na+等),而使AlCl3溶液不纯净.
(6)氯化铝水解,所以直接加热得不到氯化铝,需要在氯化氢的气氛中加热.SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体,所以根据原子守恒可知,该气体应该是二氧化氯,则反应的方程式是AlCl3?6H2O+6SOCl2=AlCl3+12HCl+6SO2↑.
解答:解:(1)根据转化图可知,固体1最终生成胆矾和铁红,这说明固体1中含有铁和铜两种元素.所以试剂A应该是氢氧化钠溶液,则生成的气体应该是铝和氢氧化钠反应生成的氢气,反应的离子方程式是2Al+2OH-+2H2O=AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=AlO2-+3H2↑;
(2)固体2最终得到胆矾,这说明固体2是铜,则试剂B不应该是碱液.根据气体2和氢氧化钠溶液反应又有气体1产生,这说明试剂B应该是硫酸,气体2中含有CO2和氢气,而溶液2中含有亚铁离子,故答案为:Fe2+;CO2和H2;
(3)固体3灼烧生成铁红,所以固体3是氢氧化铁,则溶液2转化为固体3的反应的离子方程式是4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓,故答案为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓;
(4)铜和稀硫酸不反应,但氧气能氧化单质铜生成氧化铜,进而生成硫酸铜,反应的方程式是2Cu+4H++O2
Cu2++2H2O,故答案为:2Cu+4H++O2
Cu2++2H2O;
(5)溶液1中含有偏铝酸钠,试剂C是盐酸.如果向溶液1中+加试剂C→溶液4”,则溶液4中将混有试剂A中的阳离子(如Na+等),而使AlCl3溶液不纯净;
故答案为:若在溶液1中直接加入盐酸,会使溶液4中混有试剂A中的阳离子(如Na+等),而不是纯净的AlCl3溶液;
(6)氯化铝易水解,所以直接加热得不到氯化铝,需要在氯化氢的气氛中加热;SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体,所以根据原子守恒可知,该气体应该是二氧化硫,则反应的方程式是AlCl3?6H2O+6SOCl2
AlCl3+12HCl+6SO2↑;故答案为:AlCl3?6H2O+6SOCl2
AlCl3+12HCl+6SO2↑.
(2)固体2最终得到胆矾,这说明固体2是铜,则试剂B不应该是碱液.根据气体2和氢氧化钠溶液反应又有气体1产生,这说明试剂B应该是硫酸,气体2中含有CO2和氢气,而溶液2中含有亚铁离子,故答案为:Fe2+;CO2和H2;
(3)固体3灼烧生成铁红,所以固体3是氢氧化铁,则溶液2转化为固体3的反应的离子方程式是4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓,故答案为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓;
(4)铜和稀硫酸不反应,但氧气能氧化单质铜生成氧化铜,进而生成硫酸铜,反应的方程式是2Cu+4H++O2
| ||
| ||
(5)溶液1中含有偏铝酸钠,试剂C是盐酸.如果向溶液1中+加试剂C→溶液4”,则溶液4中将混有试剂A中的阳离子(如Na+等),而使AlCl3溶液不纯净;
故答案为:若在溶液1中直接加入盐酸,会使溶液4中混有试剂A中的阳离子(如Na+等),而不是纯净的AlCl3溶液;
(6)氯化铝易水解,所以直接加热得不到氯化铝,需要在氯化氢的气氛中加热;SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体,所以根据原子守恒可知,该气体应该是二氧化硫,则反应的方程式是AlCl3?6H2O+6SOCl2
| ||
| ||
点评:本题以工艺流程图为依托,综合考查了元素化合物的性质及实验内容,试题综合性强,难易适中,侧重对学生基础知识的巩固与训练,同时也注重对学生答题能力的考查.

练习册系列答案
相关题目