题目内容
8.下列物质中属于电解质的是( )| A. | NaCl | B. | CO2 | C. | C12H22O11(蔗糖) | D. | Al |
分析 在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
在水溶液里和熔融状态下都不能导电的化合物是非电解质,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等).
解答 解:A.氯化钠在水溶液里或熔融状态下能导电的化合物是电解质,故A选;
B.二氧化碳本身不能电离,属于非电解质,故B不选;
C.C12H22O11(蔗糖)在水溶液里和熔融状态下都不能导电的化合物,是非电解质,故C不选;
D.铝为单质,既不是电解质,也不是非电解质,故D不选;
故选:A.
点评 本题考查了电解质的判断,明确电解质、非电解质概念是解题关键,注意电解质、非电解质必须是化合物,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
18.已知HClO的酸性比H2CO3弱,下列反应Cl2+H2O?HCl+HClO达到平衡后,要使平衡体系中HClO的浓度增大,应采取的方法是( )
| A. | 加入石灰石 | B. | 光照 | C. | 加入固体NaOH | D. | 加水 |
19.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | 常温下,c(NH4+)相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<④<①<③ | |
| B. | 0.2mol•L-1CH3COOH溶液与0.1mol•L-1NaOH溶液等体积混合:2c(H+)-c(CH3COO-)=2c(OH-)-c(CH3COOH) | |
| C. | pH=11氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
16.下列有关胶体的说法正确的是( )
| A. | 胶体是纯净物 | |
| B. | 胶体的分散质有可能带电,但胶体不带电 | |
| C. | 胶体、溶液与浊液的本质区别在于是否有丁达尔效应 | |
| D. | 将饱和氯化铁溶液滴入稀氢氧化钠溶液中,可得氢氧化铁胶体 |
13.有关热化学方程式书写与对应表述均正确的是( )
| A. | 稀硫酸与0.1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=+57.3 kJ•mol-1 | |
| B. | 在101KPa下氢气的燃烧热△H=-285.5 kJ•mol-1,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| C. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热为110.5 kJ•mol-1 | |
| D. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 |
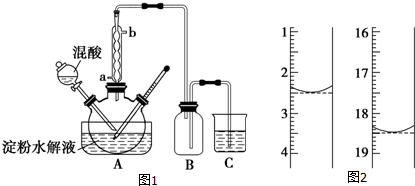
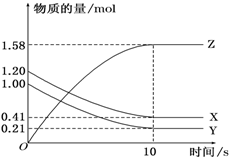 一定温度下,某1L体积固定的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:
一定温度下,某1L体积固定的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题: