题目内容
常温下,将浓度为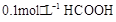 溶液加水不断稀释,下列各量始终保持增大的是( )
溶液加水不断稀释,下列各量始终保持增大的是( )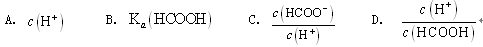
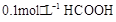 溶液加水不断稀释,下列各量始终保持增大的是( )
溶液加水不断稀释,下列各量始终保持增大的是( )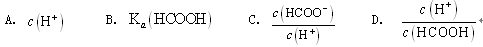
D
甲酸为弱酸,溶液中存在电离平衡:HCOOH H++HCOO-,加水稀释时,促进电离平衡的进行,故
H++HCOO-,加水稀释时,促进电离平衡的进行,故 增大;
增大;
甲酸所电离的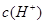 、
、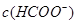 浓度将同倍数将减小,
浓度将同倍数将减小,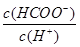 将不变;
将不变;
由于电离平衡常数只与温度有关,故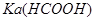 不变
不变
故答案为D
 H++HCOO-,加水稀释时,促进电离平衡的进行,故
H++HCOO-,加水稀释时,促进电离平衡的进行,故 增大;
增大;甲酸所电离的
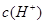 、
、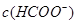 浓度将同倍数将减小,
浓度将同倍数将减小,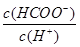 将不变;
将不变;由于电离平衡常数只与温度有关,故
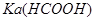 不变
不变故答案为D

练习册系列答案
相关题目

 L,pH= .
L,pH= . 体积的变化),测得混合溶液的pH=6,试回答以下问题:
体积的变化),测得混合溶液的pH=6,试回答以下问题: 2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。
2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。  字):
字): ________25 ℃。
________25 ℃。 H =11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),所得混合液为中性,求a∶b等于多少?
H =11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),所得混合液为中性,求a∶b等于多少?