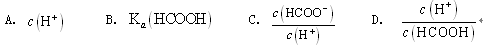题目内容
(8分)在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
(1)该温度下,水的离子积常数kw= 。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH= 。
(3)该温度下,若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,a和b之间应满足的关系是 。(列出含a、b的式子)
(4)该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因 。
(1)该温度下,水的离子积常数kw= 。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH= 。
(3)该温度下,若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,a和b之间应满足的关系是 。(列出含a、b的式子)
(4)该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因 。
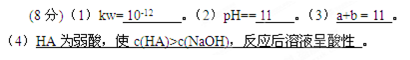
(1)该温度下,水的离子积常数
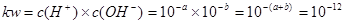 ;
;
(2)100mL0.1mol/L的稀硫酸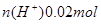 ;100mL0.4mol/L的NaOH溶液
;100mL0.4mol/L的NaOH溶液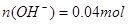 ;混合后,溶液中氢氧根离子过量,剩余物质的量为:
;混合后,溶液中氢氧根离子过量,剩余物质的量为: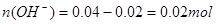 ;则
;则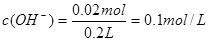 ,即
,即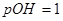 ,
,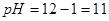 ;
;
(3)混合后溶液呈中性即酸与碱恰好完全反应,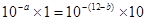 ,得
,得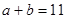 ;
;
(4)pH=2的某酸HA溶液和pH=10的NaOH溶液中氢离子浓度与氢氧根离子浓度相等,等体积混合溶液显酸性,即可得HA为弱酸;
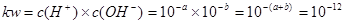 ;
;(2)100mL0.1mol/L的稀硫酸
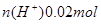 ;100mL0.4mol/L的NaOH溶液
;100mL0.4mol/L的NaOH溶液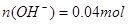 ;混合后,溶液中氢氧根离子过量,剩余物质的量为:
;混合后,溶液中氢氧根离子过量,剩余物质的量为: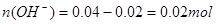 ;则
;则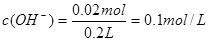 ,即
,即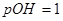 ,
,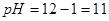 ;
;(3)混合后溶液呈中性即酸与碱恰好完全反应,
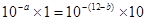 ,得
,得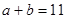 ;
;(4)pH=2的某酸HA溶液和pH=10的NaOH溶液中氢离子浓度与氢氧根离子浓度相等,等体积混合溶液显酸性,即可得HA为弱酸;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
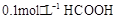 溶液加水不断稀释,下列各量始终保持增大的是( )
溶液加水不断稀释,下列各量始终保持增大的是( )