题目内容
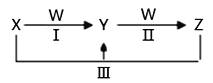
【题目】(1)已知在一定温度下,以下三个反应的平衡常数分别为K1、K2、K3:
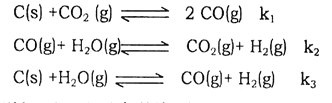
则K1、K2、K3之间的关系是K3=__________________
(2)25℃时将pH=3的强酸与pH=12的强碱溶液混合,所得溶液pH=10,则强酸与强碱的体积比是(溶液混合时体积变化忽略不计)________________
【答案】 K1×K2 9:1
【解析】(1)由①C(s)+CO2(g)2CO(g) K1
②CO(g)+H2O(g)CO2(g)+H2(g) K2
结合盖斯定律可知,①+②得到C(s)+H2O(g)CO(g)+H2(g),则K3=K1×K2;
(2)25℃时Kw=10﹣14,溶液pH=10,可知碱过量,设酸的体积为x,强碱体积为y,则![]() =10﹣4mol/L,解得x:y=9:1。
=10﹣4mol/L,解得x:y=9:1。

练习册系列答案
相关题目