题目内容
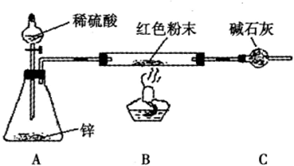
某化学小组为了测定生石膏的组成(CaSO4·xH2O),即测x值,做了如下实验:将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量.随着实验次数的增加,加热的时间不断延长,他们将实验数据整理如表3所示:
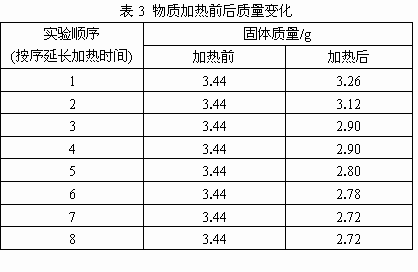
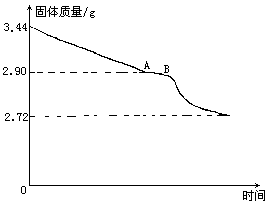
利用数据可绘制成图:
(1)利用实验数据,计算推断生石膏的化学式.
(2)通过计算解释图中产生AB段的原因.
答案:
解析:
解析:
|
(1)CaSO4·xH2O 136+18x 136 18x 3.44g 2.72g 0.72g 解得x=2,生石膏的化学式:CaSO4·2H2O. (2)从实验数据和图像知,AB段说明在生石膏受热分解过程中,有一固定组成的化合物存在,按实验数据计算 CaSO4·2H2O=CaSO4·yH2O+(2-y)H2O 172 136+18y 3.44g 2.90g 解得y=1/2, 该化合物化学式为:2CaSO4·H2O(或CaSO4·1/2H2O). 因为在加热过程中生石膏CaSO4·2H2O转化为相对稳定的2CaSO4·H2O,因此图中有AB段. |

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
 CaSO4+xH2O
CaSO4+xH2O