题目内容
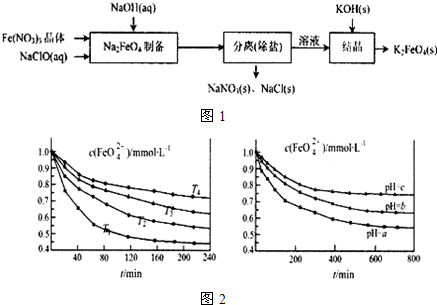
3.以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图1:
回答下列问题:
(1)写出氧化步骤中发生的主要反应的离子方程式2Fe2++H2O2+2H+═2Fe3++2H2O.
(2)如何检验中和液中的杂质离子已完全除尽?取少量中和后的溶液,滴加KSCN溶液,若溶液不变红,则已完全除去;若溶液变红,则未除尽.
(3)固体NH4Al(SO4)2•12H2O[相对分子质量:453]在加热时,固体残留率随温度的变化如图2所示.633℃时剩余固体的成分化学式为Al2(SO4)3.
(4)综上分析,流程图中M的主要成分的化学式为NH3、H2O、SO3,M可用一种物质吸收以实现循环利用,该物质的名称是浓硫酸或水.
分析 Al(OH)3、H2SO4发生反应为2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O;
工业(NH4)2SO4(含FeSO4)溶于水,然后向溶液中加入双氧水,双氧水具有氧化性、硫酸亚铁具有还原性,二者发生氧化还原反应生成铁离子和水,离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,将得到的溶液中加入氨水,调节溶液的pH,使铁离子转化为Fe(OH)3沉淀,然后过滤得到滤渣;将滤液加入硫酸铝溶液中,通过分离得到固体NH4Al(SO4)2•12H2O,加热固体NH4Al(SO4)2•12H2O,该物质分解生成M和含铝物质,
(1)双氧水和亚铁离子发生氧化还原反应生成铁离子和水;
(2)中和液中的杂质离子是铁离子,铁离子用KSCN溶液检验;
(3)633℃时剩余固体质量分数是反应前的37.75%,根据硫酸铝铵晶体分解情况分析,得出化学式;
(4)M的主要成分的化学式是NH3、H2O、SO3 ;可以用水或者浓硫酸吸收生成硫酸铵,以便重复利用.
解答 解:Al(OH)3、H2SO4发生反应为2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O;
工业(NH4)2SO4(含FeSO4)溶于水,然后向溶液中加入双氧水,双氧水具有氧化性、硫酸亚铁具有还原性,二者发生氧化还原反应生成铁离子和水,离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,将得到的溶液中加入氨水,调节溶液的pH,使铁离子转化为Fe(OH)3沉淀,然后过滤得到滤渣;将滤液加入硫酸铝溶液中,通过分离得到固体NH4Al(SO4)2•12H2O,加热固体NH4Al(SO4)2•12H2O,该物质分解生成M和含铝物质,
(1)双氧水和亚铁离子发生氧化还原反应生成铁离子和水,离子反应方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
(2)中和液中的杂质离子是铁离子,铁离子用KSCN溶液检验,其检验方法为取少量中和后的溶液,滴加KSCN溶液,若溶液不变红,则已完全除去;若溶液变红,则未除尽,
故答案为:取少量中和后的溶液,滴加KSCN溶液,若溶液不变红,则已完全除去;若溶液变红,则未除尽;
(3)假设有1mol硫酸铝铵晶体,摩尔质量是453g/mol,质量是453g,最后得到的是氧化铝,硫酸铝铵晶体加热过程中会分解,分别生成了水、氨气、三氧化硫;
当结晶水完全失去时,剩余固体与原始固体的质量百分比是:$\frac{18×12}{453}$×100%≈52.32%,大于这个值,说明结晶水没有完全失去;
当温度继续升高,硫酸铝铵中的硫酸铵开始分解生成氨气和三氧化硫,硫酸铵完全分解时,剩余物为硫酸铝,剩余固体与原始固体的质量百分比是:$\frac{171}{453}$×100%≈37.75%;当比值大于37.75%时,硫酸铵没有完全分解,当等于这个比值,说明硫酸铵恰好分解完全,小于这个比值,硫酸铝开始分解;故B点剩余固体是硫酸铝;
故答案是:Al2(SO4)3;
(4)根据(3)知,流程图中M的主要成分的化学式为NH3、H2O、SO3 ;可以用水或者浓硫酸吸收生成硫酸铵重复使用;
故答案是:NH3、H2O、SO3;浓硫酸或水.
点评 本题考查物质制备实验方案评价,为高频考点,侧重考查学生分析、推断、计算能力,明确流程图中发生的反应及基本操作是解本题关键,难点是(3)题有关计算,题目难度中等.

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案| A. | A与B两种气体的相对分子质量之比为a:b | |
| B. | 同质量的A、B两种气体分子数之比为b:a | |
| C. | 同温同压时,两种气体A与B的密度之比为a:b | |
| D. | 同温同体积时,同质量的A、B两种气体的压强之比为a:b |
| A. | 向CuSO4溶液中加入NaOH溶液得到的分散系 | |
| B. | 向水中加入食盐得到的分散系 | |
| C. | 向沸水中滴入饱和FeCl3溶液得到的红褐色液体 | |
| D. | 向NaOH溶液中通入CO2得到的无色溶液 |
 )甲酯并计算其产率.实验步骤如下:
)甲酯并计算其产率.实验步骤如下:Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,以及约10mL甲苯(甲苯与
 水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯5.3g.
常用物理常数如下:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)实验中加入沸石的作用是防暴沸;
(3)加入甲苯的作用是将反应产生的水从反应体系中分离出来,使合成水杨酸甲酯反应的化学平衡向右移动,从而提高反应的产率.
(4)反应结束后,分离甲醇所采用操作的名称是蒸馏.
(5)洗涤操作中,前后两次水洗的目的分别是为了洗掉洗掉大部分硫酸和洗掉碳酸氢钠.
(6)在蒸馏操作中,仪器选择及安装都正确的是(填标号)b.

(7)本实验的产率为70%(保留两位有效数字).
| A. | 0.1mol/L的醋酸溶液中c(H+)=0.1mol/L | |
| B. | 0.1mol/L 的NaClO溶液中pH>7 | |
| C. | 任何一个化学变化都伴随着能量的变化 | |
| D. | 新制的氯水中存在着三种分子 |
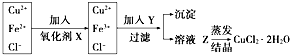 工业上制取纯净的CuCl2•2H2O的主要过程是:
工业上制取纯净的CuCl2•2H2O的主要过程是:
 (g)+CO2(g)?
(g)+CO2(g)? (g)+CO(g)+H2O(g)△H=-166KJ/mol
(g)+CO(g)+H2O(g)△H=-166KJ/mol