题目内容
14.铟产业被称为“信息时代的朝阳产业”.元素周期表中铟的数据如图,下列说法完全正确的是( )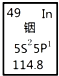
| A. | 铟元素的质量数是114.8 | |
| B. | 铟元素的相对原子质量是114 | |
| C. | 铟原子最外层有3个能量相同的电子 | |
| D. | 铟元素是一种主族元素 |
分析 A.具有一定质子数的一类原子是总称是元素,元素不说质量数;
B.元素周期表中外围电子排布下方的数值为元素的相对原子质量;
C.铟的核外电子排布中有5s,那么该元素位于第五周期,p上1个电子,最外层电子数为2+1=3,处于第ⅢA族;
D.能级不同,其电子能量不同.
解答 解:A.质量数是将原子内所有质子和中子的相对质量取近似整数值相加而得到的数值,元素周期表中外围电子排布下方的数值为元素的相对原子质量,该元素的相对原子质量是114.8,故A错误;
B.元素周期表中外围电子排布下方的数值为元素的相对原子质量,该元素的相对原子质量是114.8,故B错误;
C.能级不同,其电子能量不同,所以5s、5p能级上电子能量不同,故C错误;
D.铟的核外电子排布中有5s,那么该元素位于第五周期,p上1个电子,最外层电子数为2+1=3,处于第ⅢA族,故D正确;
故选:D.
点评 本题考查了元素周期表的结构及应用,明确图中各个数字或字母代表的含义是解本题关键,注意114.8是该元素的相对原子质量而不是铟元素中某一种原子的相对原子质量,为易错点.

练习册系列答案
相关题目
4.分别处于第二、三周期的主族元素A和B,它们的离子的电子层相差2层.已知A处于第m族;B处于第n族;A只有正化合价.则A、B原子核外电子总数分别为( )
| A. | m、n | B. | 3、7 | C. | m-2、10n | D. | m+2、n+10 |
5.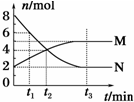 一定温度下,在容积为2L的容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,则下列表述中正确的是( )
一定温度下,在容积为2L的容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,则下列表述中正确的是( )
 一定温度下,在容积为2L的容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,则下列表述中正确的是( )
一定温度下,在容积为2L的容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,则下列表述中正确的是( )| A. | 该反应的化学方程式为2M?N | |
| B. | t2时,正、逆反应速率相等,达到平衡 | |
| C. | t2时,用M表示的反应速率为$\frac{1}{{t}_{2}}$mol•L-1•min-1 | |
| D. | t3时,每生成1mol M的同时会生成1mol N |
2.下列过程中所发生的化学变化属于取代反应的是( )
| A. | 乙烯通入溴水中 | |
| B. | 光照射甲烷与氯气的混合气体 | |
| C. | 在镍作催化剂的条件下,苯与氢气反应 | |
| D. | 乙醇与酸性重铬酸钾溶液反应 |
9.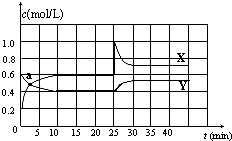 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )
 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )| A. | 图中的两条曲线,X是表示NO2浓度随时间的变化曲线 | |
| B. | a点时v(N2O4)=v(NO2) | |
| C. | 25min时改变了影响速率的一个因素,使得NO2转变为N2O4,该改变是将密闭容器的体积缩小,增大压强 | |
| D. | 前10min内用v(N2O4)表示的化学反应速率为0.02 mol/(L•min) |
19.将NO2、NH3、O2的混和气体22.4升通过稀硫酸后,溶液的质量增加23.6克,气体体积缩小为4.48升(气体体积均在标准状况下测定),剩余气体能使带余烬的木条复燃,则混和气体的平均相对分子质量为( )
| A. | 28 | B. | 30 | C. | 32 | D. | 34 |
6.对于Na+、Mg2+、Al3+三种离子,下列说法不正确的是( )
| A. | 核外电子层数相同 | B. | 半径大小顺序Na+<Mg2+<Al3+ | ||
| C. | 核外电子数相同 | D. | 最外层电子数相同 |
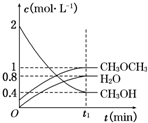 二甲醚(CH3OCH3)是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5J•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.
二甲醚(CH3OCH3)是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5J•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.