题目内容
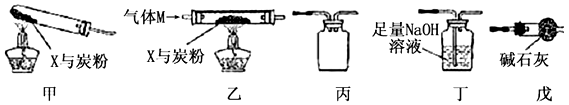
固体粉末X由Fe2O3 、CuO组成,某研究性学习小组选用图17中装置(夹持装置已略去,实验前均已检查装置气密性)探究X与过量炭粉发生反应时,除生成![]() 外,是否还有其他气体产物。
外,是否还有其他气体产物。
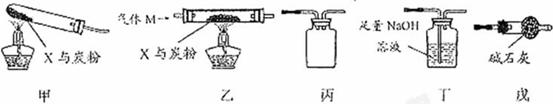
图17
请回答:
(1)若按甲→丙→丁的顺序连接装置,则____________________(填上图装置代号)装置和试剂需称量,开始反应,气体经充分吸收后,分析数据发现,消耗碳、氧元素的质量大于生成![]() 的质量,可能的原因除产生了
的质量,可能的原因除产生了![]() 外的其他气体产物,还可能是____ _____________.
外的其他气体产物,还可能是____ _____________.
(2)为使实验测得的数据更能准确说明问题,一些同学按乙→丁→戊的顺序连接装置进行实验,并且加热前先通一会气体M,停止加热后再通一会儿该气体。
①气体M可能是____________ (填字母)。
a.![]() b.
b.![]() c.
c.![]() d.CO e.
d.CO e.![]()
②停止加热后再通一会气体M的原因是_________________________________________。
(3)以上两套装置均存在的同样的明显缺陷是____________________________________。
(4)该小组同学设计实验(如图18)将X进行转化(每一步均反应完全):
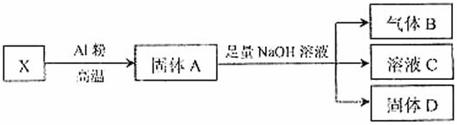
图18
①生成气体B的化学方程式是___________________________________________ 。
②将固体D投入过量稀硫酸并充分反应后,过滤,再向滤液加入双氧水,得黄色溶液。
写出当加入双氧水时溶液中发生反应的离子方程式:
____________________________________________________________。
③若已知固体X的质量为7.2g反应中AI粉的质量是2.7g,气体B在标准状况下的体积为672ml,则固体D的质量是_________ g.
(1)甲、丁 生成CO2气体残留在装置中
(2)①c ②将装置中残留的CO2气体吹出;防止溶液发生倒吸
(3)无尾气处理装置
(4)①2Al+2NaOH+2H2O=2NaAlO+3H2↑
②2Fe2++H2O2+2H+=2Fe2++2H2O
③5.28

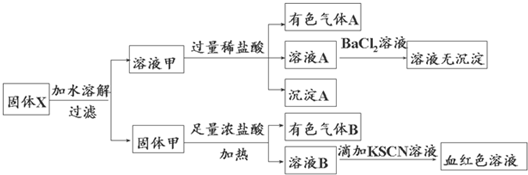
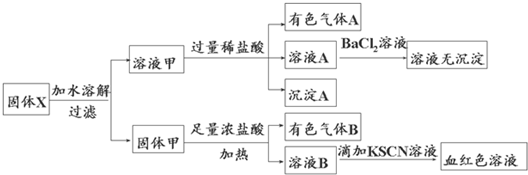
根据上述实验,以下说法正确的是( )
| A、溶液甲中一定含有K2SiO3、NaNO2、可能含有KAlO2、K2CO3 | B、由于在溶液甲中加入足量稀盐酸后再加入BaCl2溶液,因此无法判断溶液中是否有K2SO3 | C、气体A和气体B一定均为纯净物 | D、原混合物中一定含有Fe2O3 |