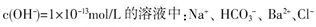题目内容
下列叙述或表示正确的是
| A.0.1 mol·L-1的醋酸的pH=a,0.01 mol·L-1的醋酸的pH=b,则a+1=b |
| B.常温下0.1 mol·L-1的醋酸溶液与等浓度等体积NaOH溶液反应后的溶液中:c(CH3COOH)+c(CH3COOˉ)="0.1" mol·L-1 |
| C.难溶电解质AB2的饱和溶液中,c(A2+)=xmol·L-1, c(B-)="y" mol·L-1,则Ksp值为4xy2 |
| D.用200mL4 mol·L-1的NaOH溶液将0.6mol CO2完全吸收,反应的离子方程式为:3CO2+4OHˉ=CO32ˉ+2HCO3ˉ+H2O |
D
试题分析:A、浓度不同的醋酸电离程度不同,,浓度越小电离程度越大,故a+1>b;B、0.1 mol·L-1的醋酸溶液与等浓度等体积NaOH溶液反应后得醋酸钠溶液,根据物料守恒可得醋酸根离子和醋酸分子的浓度之和等于钠离子的浓度,为0.05 mol·L-1,故B错误;根据Ksp的表达式可知,应为xy2,故C错误;根据氢氧化钠和二氧化碳的物质的量分别为0.8mol和0.6mol,根据化学方程式计算可得生成碳酸钠和碳酸氢钠的物质的量分别为0.2mol和0.4mol,根据量判断出方程式中的系数,写出离子方程式,故D正确。

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
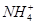 )>c(H+)=c(OH-)
)>c(H+)=c(OH-)