题目内容
【题目】元素周期表的形式多种多样,图是扇形元素周期表的一部分,对比中学常见元素周期表,分析其元素的填充规律,判断下列说法正确的是( ) 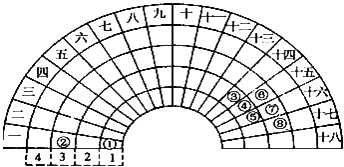
A.③元素形成的单质晶体均属于原子晶体
B.②、⑦、⑧对应的简单离子半径依次减小
C.②⑤形成的化合物阴阳离子个数比可能为1:1
D.④元素的气态氢化物易液化,是因为其分子间存在氢键
【答案】D
【解析】解:由元素在周期表中的位置可知,①为H、②为Na、③为C、④为N、⑤为O、⑥为P、⑦为S、⑧为Cl.
A.碳单质中金刚石为原子晶体,石墨为混合晶体,而C60等为分子晶体,故A错误;
B.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2﹣>Cl﹣>Na+ , 故B错误;
C.Na2O与Na2O2中阴阳离子个数比均为1:2,故C错误;
D.氨气分子之间存在氢键,沸点较高,容易液化,故D正确.
故选D.

练习册系列答案
相关题目