题目内容
9.某可逆反应:X(g)+Y(g)?Z(g),其正反应的活化能小于逆反应的活化能.下列示意图中,虚线能正确表示反应在催化剂作用下能量变化与反应过程关系的是( )| A. | 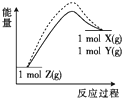 | B. |  | C. |  | D. | 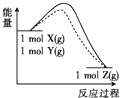 |
分析 在催化剂作用下,反应的活化能小于非催化作用下反应的活化能,故A、C两项错误;
又由反应:X(g)+Y(g) Z(g)正反应的活化能小于逆反应的活化能,可知该反应正方向为放热过程,据此分析.
Z(g)正反应的活化能小于逆反应的活化能,可知该反应正方向为放热过程,据此分析.
解答 解:在催化剂作用下,反应的活化能小于非催化作用下反应的活化能,故A、C两项错误;
又由反应:X(g)+Y(g) Z(g)正反应的活化能小于逆反应的活化能,可知该反应正方向为放热过程,则反应物总能量大于生成物总能量,故D项正确;
Z(g)正反应的活化能小于逆反应的活化能,可知该反应正方向为放热过程,则反应物总能量大于生成物总能量,故D项正确;
故选:D.
点评 本题考查了化学反应的能量变化分析,催化剂的作用实质,图象识别和理解含义是解题关键.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
19.化学反应2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C的反应类型是( )
| A. | 化合反应 | B. | 置换反应 | C. | 分解反应 | D. | 复分解反应 |
20.在一个绝热且容积不变的密闭容器中,发生如下反应:
C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ•mol-1
下列一定能说明该反应已经达到平衡状态的有( )
C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ•mol-1
下列一定能说明该反应已经达到平衡状态的有( )
| A. | c(CO)=c(H2) | |
| B. | 单位时间内断裂2个H-O键的同时生成了1个H-H键 | |
| C. | 容器内反应温度不再改变 | |
| D. | 容器内的混合气体密度保持不变 |
17.下列常见金属的冶炼原理不正确的是( )
| A. | Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe | B. | MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | ||
| C. | 2AlCl3$\frac{\underline{\;通电\;}}{\;}$2Al+3Cl2↑ | D. | 2Ag2O$\frac{\underline{\;\;△\;\;}}{\;}$4Ag+O2↑ |
4.在MgCl2和AlCl3的混合溶液中,Cl-的物质的量为0.7mol,Al3+与Mg2+的物质的量之比为1:2.向该溶液中逐渐加入100mL 8mol•L-1 NaOH溶液,使之充分反应.下列叙述不正确是( )
| A. | 溶液中MgCl2的物质的量为0.1 mol | |
| B. | 当加入87.5 mL NaOH溶液时,沉淀质量最大 | |
| C. | 当加入90.0 mL NaOH溶液时,溶液中NaAlO2与NaCl的物质的量之比为2:35 | |
| D. | 当100 mL NaOH溶液刚好完全消耗时,Al3+恰好全部转化为Al${O}_{2}^{-}$ |
14.已知:P4(s)+6Cl2(g)═4PCl3(g)△H=a kJ•mol-1,P4(s)+10Cl2(g)═4PCl5(g)△H=b kJ•mol-1;破坏PCl5中1mol P-Cl键所需能量为c kJ•mol-1,破坏PCl3中1mol P-Cl键所需能量为1.2c kJ•mol-1.则破坏Cl2中 1mol Cl-Cl键所需的能量为( )
| A. | $\frac{a+b}{4}$ kJ•mol-1 | B. | $\frac{b-a+c}{4}$ kJ•mol-1 | ||
| C. | $\frac{b-a+5.6c}{4}$ kJ•mol-1 | D. | $\frac{5a-3b+12c}{8}$ kJ•mol-1 |
19.下列条件下,两种气体的分子数一定不相等的是( )
| A. | 相同质量、不同密度的N2O和CO2 | |
| B. | 相同体积、相同密度的CO和C2H4 | |
| C. | 相同温度、相同压强、相同体积的O2和N2 | |
| D. | 相同压强、相同体积、相同质量的NO2和N2O5 |