题目内容
(1)用热水配制AlCl3溶液,会出现浑浊现象,原因是(用离子方程式和必要的文字说明):
。要消除浑浊现象,又不污染药品,可加入适量的__________溶液。
(2)常温下,有①0.01 mol/L HCl溶液;②pH=12的氨水,其中水的电离程度① ②,(选填“>”、“<”或“=”);若将①、②混合后所得溶液pH=7,则消耗溶液的体积:① ②(选填“>”、“<”或“=”)。若用①来滴定未知浓度的氨水,通常选用____________作指示剂,达滴定终点时各离子浓度由大到小的顺序是_________________________________。
(3)某温度(T℃)时,测得0.01 mol·L-1NaOH溶液的pH=11,则在该温度下,将100 mL 0.2 mol·L-1的稀盐酸与100 mL 0.4 mol·L-1的NaOH溶液混合后,溶液的pH= 。
。要消除浑浊现象,又不污染药品,可加入适量的__________溶液。
(2)常温下,有①0.01 mol/L HCl溶液;②pH=12的氨水,其中水的电离程度① ②,(选填“>”、“<”或“=”);若将①、②混合后所得溶液pH=7,则消耗溶液的体积:① ②(选填“>”、“<”或“=”)。若用①来滴定未知浓度的氨水,通常选用____________作指示剂,达滴定终点时各离子浓度由大到小的顺序是_________________________________。
(3)某温度(T℃)时,测得0.01 mol·L-1NaOH溶液的pH=11,则在该温度下,将100 mL 0.2 mol·L-1的稀盐酸与100 mL 0.4 mol·L-1的NaOH溶液混合后,溶液的pH= 。
(1)Al3++3H2O 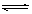 Al(OH)3+3H+由于加热会促进Al3+的水解,同时产生的HCl受热逸出,故用热水配制时水解产生的Al(OH)3增多会出现浑浊现象(3分)
Al(OH)3+3H+由于加热会促进Al3+的水解,同时产生的HCl受热逸出,故用热水配制时水解产生的Al(OH)3增多会出现浑浊现象(3分)
HCl(1分)
(2)=(2分) >(2分)甲基橙(2分)c(Cl-)>c(NH4+)>c(H+)>c(OH-) (2分)
(3)pH=12(2分)
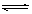 Al(OH)3+3H+由于加热会促进Al3+的水解,同时产生的HCl受热逸出,故用热水配制时水解产生的Al(OH)3增多会出现浑浊现象(3分)
Al(OH)3+3H+由于加热会促进Al3+的水解,同时产生的HCl受热逸出,故用热水配制时水解产生的Al(OH)3增多会出现浑浊现象(3分)HCl(1分)
(2)=(2分) >(2分)甲基橙(2分)c(Cl-)>c(NH4+)>c(H+)>c(OH-) (2分)
(3)pH=12(2分)
(1)原因:铝离子水解,Al3++3H2O Al(OH)3↓+3H+ 温度升高,Al3+水解程度增大,要消除浑浊现象,又不污染药品,可加入适量的盐酸,抑制Al3+水解。
Al(OH)3↓+3H+ 温度升高,Al3+水解程度增大,要消除浑浊现象,又不污染药品,可加入适量的盐酸,抑制Al3+水解。
(2)水的电离程度①=②,因为溶液中c(H+)=c(OH-)
若将①、②混合后所得溶液pH=7,则消耗溶液的体积:①>②,因为氨水的浓度大于盐酸的浓度,盐酸体积应该多些。
若用①来滴定未知浓度的氨水,通常选用甲基橙作指示剂,因为滴定终点显酸性
达滴定终点时各离子浓度由大到小的顺序是:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(3)pH=12
 Al(OH)3↓+3H+ 温度升高,Al3+水解程度增大,要消除浑浊现象,又不污染药品,可加入适量的盐酸,抑制Al3+水解。
Al(OH)3↓+3H+ 温度升高,Al3+水解程度增大,要消除浑浊现象,又不污染药品,可加入适量的盐酸,抑制Al3+水解。(2)水的电离程度①=②,因为溶液中c(H+)=c(OH-)
若将①、②混合后所得溶液pH=7,则消耗溶液的体积:①>②,因为氨水的浓度大于盐酸的浓度,盐酸体积应该多些。
若用①来滴定未知浓度的氨水,通常选用甲基橙作指示剂,因为滴定终点显酸性
达滴定终点时各离子浓度由大到小的顺序是:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(3)pH=12

练习册系列答案
相关题目
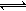 HCO3-+H+的Ka=10-6.1,正常血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3,lg5=0.7。则下列判断正确的是( )
HCO3-+H+的Ka=10-6.1,正常血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3,lg5=0.7。则下列判断正确的是( )