题目内容
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1;反应的平衡常数K1为_____________。

(2)100 ℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。T______100 ℃(填“大于”或“小于”),判断理由是____________________________________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是____________________________________。
【答案】 大于 0.0010 0.36 mol·L-1 大于 反应正方向吸热,反应向吸热方向进行,故温度升高 逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动
【解析】(1)温度升高,混合气体的颜色变深,说明平衡向正反应方向进行,因此正反应是吸热反应,则反应的ΔH大于0;在0~60 s时段内消耗四氧化二氮的物质的量浓度为0.1mol/L-0.040mol/L=0.06mol/L,因此反应速率v(N2O4)=0.06mol/L÷60s=0.0010mol·L-1·s-1;平衡时N2O4、NO2的浓度分别是0.04mol/L、0.12mol/L,则反应的平衡常数K1为![]() 。(2)c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,说明平衡向正反应方向进行,由于正反应吸热,所以改变的条件是升高温度,即T大于100 ℃;(3)由于正反应体积增大,所以对气体分子数增大的反应,增大压强平衡向逆反应方向移动。
。(2)c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,说明平衡向正反应方向进行,由于正反应吸热,所以改变的条件是升高温度,即T大于100 ℃;(3)由于正反应体积增大,所以对气体分子数增大的反应,增大压强平衡向逆反应方向移动。

 名题金卷系列答案
名题金卷系列答案【题目】下列各选项中,可用右侧示意图表示的是
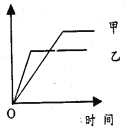
反应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量氨,在同一容器中:2NH3 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量的钾、钠分别与水反应 | H2的质量 | 钠 | 钾 |
C | 体积比为1︰3的N2、H2,在体积可变的恒压容器中: N2+3H2 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2mol SO2与1mol O2,在相同温度下:2SO2+O2 | SO3的物质的量 | 10 MPa | 20 MPa |
A. A B. B C. C D. D