题目内容
【题目】如图,a、b是石墨电极,通电一段时间后,a极附近溶液显红色。下列说法正确的是( )
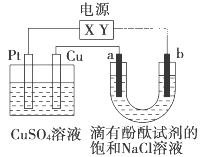
A. Pt极上有64 g Cu析出时,b极产生22.4 L气体
B. a极的电极反应是2Cl--2e-= Cl2↑
C. 电解过程中CuSO4溶液的pH逐渐增大
D. X极是电源负极,Y极是电源正极
【答案】D
【解析】a、b是石墨电极,通电一段时间后,a极附近溶液显红色,说明有氢氧根产生,即a电极是阴极,b是阳极,则Y是电源的正极,X是负极,Pt电极是阴极,铜电极是阳极。A、电解过程中硝酸铜溶液中的铜离子在Pt电极得到电子析出铜,物质的量是1mol,转移2mol电子,b电极是阳极,氯离子放电,根据电子得失守恒可知氯气是1mol,标准状况下是22.4L,A错误;B、a电极是氢离子放电,B错误;C、左池相当于是Pt电极上镀铜,因此电解过程中硫酸铜溶液的pH不变,C错误;D、根据以上分析可知X极是电源负极,Y极是电源正极,D正确,答案选D。

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
【题目】探究:1-氯丙烷与NaOH乙醇溶液的反应
学习小组在进行1-氯丙烷与NaOH乙醇溶液溶液的反应中,观察到有气体生成。
请你设计两种不同的方法分别检验该气体。在表中的方框中写出装置中所盛试剂的名称(试剂任选) 和实验现象。
图序 | 装置图 | 所盛试剂 | 实验现象 |
1 |
| A是_________ B是_________ | _________ |
2 |
| C是_______________ | _________ |