题目内容
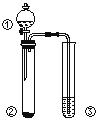
【题目】液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是

A. 电流从右侧电极经过负载后流向左侧电极
B. 负极发生的电极反应式为N2H4+4OH--4e-===N2+4H2O
C. 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D. 该燃料电池持续放电时,正极发生氧化反应,pH减小
【答案】D
【解析】
该燃料电池中,负极上燃料失电子发生氧化反应,左侧为负极,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,正极上氧气得电子发生还原反应,右侧为正极,电极反应式为:O2+2H2O+4e-=4OH-,电池总反应为:N2H4+O2=N2↑+2H2O,结合原电池的工作原理可得结论。
A.该燃料电池中,右侧通入氧化剂空气的电极为正极,电流从正极流向负极,即电流从右侧电极经过负载后流向左侧电极,故A叙述正确;
B.通入燃料的电极为负极,负极上燃料失电子发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,故B叙述正确;
C.因为电池中正负极上为气体参与的反应,所以采用多孔导电材料,可以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触,故C叙述正确;
D.该燃料电池持续放电时,正极上氧气得电子发生还原反应,放电过程中生成水,电解质溶液KOH的浓度减小,pH减小,故D叙述错误;
答案选D。

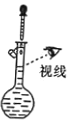
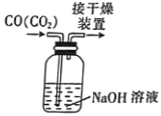
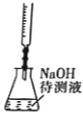
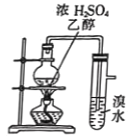
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性: C>Si | |
B | 食盐水 | 电石 | 溴水 | 乙炔可与溴发生加成反应 | |
C | 浓硝酸 | Al | NaOH溶液 | 铝和浓硝酸反应可生成NO2 | |
D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | SO2具有还原性 |
A. A B. B C. C D. D
【题目】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) △H1=+551kJmol-1
反应Ⅲ:S(g)+O2(g)=SO2(g) △H3=-297kJmol-1
反应Ⅱ的热化学方程式:____________________。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如右图所示,p2______p1(填“>”或“<”),得出该结论的理由是__________。

(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下,将ii补充完整
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+______=______+______+2I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象,(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4molL-1 KI | amolL-1 KI 0.2molL-1H2SO4 | 0.2molL-1H2SO4 | 0.2molL-1 KI 0.0002 molI2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
① B是A的对比实验,则a=______。
②比较A、B、C,可得出的结论是______。
③实验表明,SO2的歧化反应速率D>A.结合i,ii反应速率解释原因:______。