题目内容
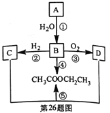
【题目】烃A是一种重要的化工原料。己知A在标准状况下的密度为1.16g·L-1,B可发生银镜反应。它们之间的转化关系如图:请回答:
(1)有机物A中含有的官能团名称是____________。
(2)反应④的原子利用率达100%,该反应的化学方程式是___________。
(3)下列说法正确的是___________。
A 反应⑤合成乙酸乙酯也能实现原子利用率100%
B.反应②、③、⑤的类型各不相同
C 由于乙酸乙酯和水均为无色液体,故用分液漏斗无法分离乙酸乙酯和水的混合物
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全
【答案】碳碳叁键 2CH3CHO![]() CH3COOCH2CH3 BD
CH3COOCH2CH3 BD
【解析】
A在标准状况下的密度为1.16gL-1,则A的摩尔质量为1.16g/L×22.4L/mol=26g/mol,B可发生银镜反应,则B为醛,由流程图可知,A加水反应生成B,B氧化生成D,B加氢还原生成C,C与D发生反应生成乙酸乙酯,则A为CH≡CH,B为CH3CHO,C为CH3CH2OH,D为CH3COOH,以此来解答。
(1)由上述分析可知,A为CH≡CH,官能团名称为碳碳叁键,故答案为:碳碳叁键;
(2)由上述分析可知,B为CH3CHO,反应④的原子利用率达100%,则CH3CHO发生加成反应生成CH3COOCH2CH3,该反应的化学方程式是2CH3CHO![]() CH3COOCH2CH3,故答案为:2CH3CHO
CH3COOCH2CH3,故答案为:2CH3CHO![]() CH3COOCH2CH3 ;
CH3COOCH2CH3 ;
(3)A. C为CH3CH2OH与乙酸发生酯化反应生成乙酸乙酯和水,为可逆反应,则在一定条件下合成乙酸乙酯不能实现原子利用率100%,故A错误;
B.反应②为还原反应,③为氧化反应、⑤为酯化反应,所以类型各不相同,故B正确;
C.乙酸乙酯与水不相溶,可以用分液漏斗分离乙酸乙酿和水的混合物,故C错误;
D.乙酸乙酯在氢氧化钠溶液中水解生成乙酸钠和乙醇,不可逆,较在稀硫酸中更完全,故D正确;
故选BD。

 名校课堂系列答案
名校课堂系列答案