题目内容
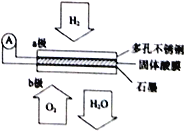
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B. 放电时正极反应为:FeO42-+4H2O + 3e-=Fe(OH)3+5OH-
C. 放电时每转移3mol电子,正极有1mol K2FeO4被还原
D. 放电时正极附近溶液的pH不变
【答案】D
【解析】
A、放电时,Zn作负极,被氧化,由总反应可得,生成Zn(OH)2,电解质溶液呈碱性,所以电极反应式为Zn-2e-+2OH-=Zn(OH)2,A正确;
B、放电时,K2FeO4为电池的正极,发生还原反应,生成Fe(OH)3,电极反应式为FeO42-+4H2O+3e-=Fe(OH)3+5OH-,B正确;
C、放电时,K2FeO4为电池的正极,Fe的化合价由+6价降为+3价,则每转移3mol电子,正极有1molK2FeO4被还原,C正确;
D、放电时,K2FeO4为电池的正极,发生还原反应,生成Fe(OH)3,电极反应式为FeO42-+4H2O+3e-=Fe(OH)3+5OH-,正极生成OH-,溶液碱性增强,pH增大,D错误。
答案选D。

 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案【题目】Ⅰ.有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究X的组成与结构,进行了如下实验:
(1)有机物X的质谱图为: | |
| 有机物X的相对分子质量是________。 |
(2)将10.0 g X在足量O2中充分燃烧,并使其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。 | 有机物X的分子式是______。 |
(3)经红外光谱测定,有机物X中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3∶1。 | 有机物X的结构简式是__________。 |
II.写出与![]() 互为同分异构体,且一溴代物只有两种的芳香烃的结构简式和名称:________________、___________。
互为同分异构体,且一溴代物只有两种的芳香烃的结构简式和名称:________________、___________。