题目内容
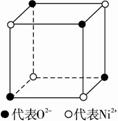
⑴中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧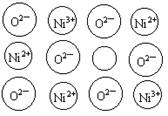 化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2―的核间距离为a×10―8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g/mol)
化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2―的核间距离为a×10―8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g/mol)
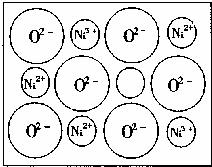
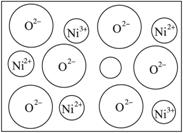
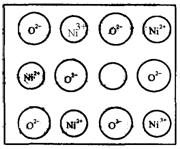
(2)天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。
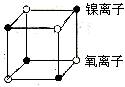
⑴ 因NiO与NaCl的晶体结构相似,所以在NiO的晶胞(如图所示)中含NiO微粒数为1/2个,其晶体的密度为:
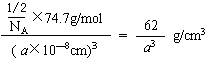
⑵ 设1mol Ni0.97O中含Ni3+x mol,,Ni2+(0.97-x)mol
根据电中性:3x mol + 2(0.97-x)mol=2×1mol ,则x=0.06
Ni2+为(0.97-x)mol=0.91
离子数之比 Ni3+:Ni2+=0.06:0.91=6:91

练习册系列答案
相关题目
 (1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体. NiO(氧化镍〕晶体的结构与NaQ相同,Ni2+与最邻近O2-的核间距离为a10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g.mol-1).
(1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体. NiO(氧化镍〕晶体的结构与NaQ相同,Ni2+与最邻近O2-的核间距离为a10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g.mol-1).
 (1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体结构与NaCl相同,Ni2+与最邻近的O2—的核间距离为a×10-8cm,计算NiO晶体的密度。(已知NiO的摩尔质量为:74.7g·mol-1)
(1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体结构与NaCl相同,Ni2+与最邻近的O2—的核间距离为a×10-8cm,计算NiO晶体的密度。(已知NiO的摩尔质量为:74.7g·mol-1)