题目内容
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
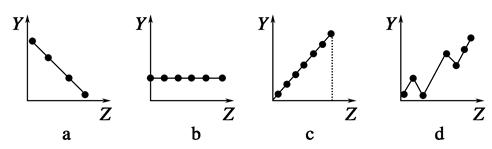
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为________(名称),Y为________(元素符号),Z原子结构示意图为________。
②N的最高价氧化物的水化物的化学式为__________。
③工业上制取单质M的化学方程式为______________。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:

①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为________(名称),Y为________(元素符号),Z原子结构示意图为________。
②N的最高价氧化物的水化物的化学式为__________。
③工业上制取单质M的化学方程式为______________。
(1)①b ②c ③a
(2)①氢 O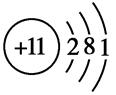 ②HClO4 ③SiO2+2C
②HClO4 ③SiO2+2C Si+2CO↑
Si+2CO↑
(2)①氢 O
 ②HClO4 ③SiO2+2C
②HClO4 ③SiO2+2C Si+2CO↑
Si+2CO↑(1)①第ⅡA族元素的价电子数都是2,b符合。
②第三周期元素的最高化合价从+1价逐渐增大到+7价,c符合。
③F-、Na+、Mg2+、Al3+的离子半径为F->Na+>Mg2+>Al3+,a符合。
(2)已知Y原子最外层电子数与核外电子总数之比为3∶4,则Y为O。M元素原子的最外层电子数与电子层数之比为4∶3,则M为Si。由X、Y、Z、M、N的原子序数关系和N、Z、X的简单离子形式可知,N为Cl,Z为Na,X为H。
②第三周期元素的最高化合价从+1价逐渐增大到+7价,c符合。
③F-、Na+、Mg2+、Al3+的离子半径为F->Na+>Mg2+>Al3+,a符合。
(2)已知Y原子最外层电子数与核外电子总数之比为3∶4,则Y为O。M元素原子的最外层电子数与电子层数之比为4∶3,则M为Si。由X、Y、Z、M、N的原子序数关系和N、Z、X的简单离子形式可知,N为Cl,Z为Na,X为H。

练习册系列答案
相关题目

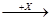 乙
乙 丙,若其中甲是单质,乙、丙为化合物,x是具有氧化性的无色气体单质,则甲的化学组成不可能是________(选填序号,下同)。
丙,若其中甲是单质,乙、丙为化合物,x是具有氧化性的无色气体单质,则甲的化学组成不可能是________(选填序号,下同)。
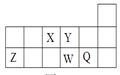
 ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。