题目内容
12.下列关于分子式为C6H12O2的有机物的同分异构体的说法中,不正确的是( )| A. | 若可以水解,且能发生银镜反应,则其同分异构有8种 | |
| B. | 若可以与碳酸氢钠溶液反应生成CO2,则其同分异构有8种 | |
| C. | 一定能与Na反应生成H2 | |
| D. | 可能与NaOH溶液反应 |
分析 A.可以水解,且能发生银镜反应,应为甲酸形成的酯;
B.可以与碳酸氢钠溶液反应生成CO2,则含有-COOH;
C.如为酯类,则与钠不反应;
D.可为酸或酯类,都可与氢氧化钠反应.
解答 解:A.可以水解,且能发生银镜反应,应为甲酸形成的酯,则对应的醇为C5H11OH,-C5H11有8种同分异构体:CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,故A正确;
B.可以与碳酸氢钠溶液反应生成CO2,则含有-COOH,则含有,由A分析可知-C5H11同分异构体有8种,故B正确;
C.如为酯类,则与钠不反应,故C错误;
D.分子式为C6H12O2的有机物可为酸或酯类,都可与氢氧化钠反应,故D正确.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物官能团的性质以及同分异构体的判断,难度中等.

练习册系列答案
相关题目
3.常见的污染物分为一次污染物和二次污染物.二次污染物是指排入环境中的一次污染物在物理化学因素或微生物作用下发生变化所生成的新污染物.如反应2NO+O2═2NO2中,二氧化氮为二次污染物,下列物质中不会导致二次污染的是( )
①SO2 ②NO ③NO2 ④HCl ⑤CO2.
①SO2 ②NO ③NO2 ④HCl ⑤CO2.
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ④⑤ | D. | ④ |
3.部分中学化学常见元素原子结构及性质如表所示:
(1)A元素在周期表中的位置为第四周期Ⅷ族
(2)B与C形成的化合物的化学式为Mg3N2,写出电子式
(3)①C与F组成的5核阳离子的鉴别方法加入浓NaOH溶液加热,生成气体若能够使湿润的红色石蕊试纸变蓝,说明含有铵根离子
②C与F组成18电子化合物结构式为
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱4NH3+3O2(纯)$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O
(5)工业制备D的粗产品的化学反应方程式为SiO2+2C═Si+2CO↑.
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种常见氯化物,相对分子质量相差35.5 |
| ② | B | B原子最外层电子数是内层电子总数的$\frac{1}{5}$ |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ | E | 通常情况下,E没有最高正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(2)B与C形成的化合物的化学式为Mg3N2,写出电子式

(3)①C与F组成的5核阳离子的鉴别方法加入浓NaOH溶液加热,生成气体若能够使湿润的红色石蕊试纸变蓝,说明含有铵根离子
②C与F组成18电子化合物结构式为

(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱4NH3+3O2(纯)$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O
(5)工业制备D的粗产品的化学反应方程式为SiO2+2C═Si+2CO↑.
20.某有机物 的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )
的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )
 的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )
的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
7.分子式为C4H10O的醇与分子式为C8H8O2且含苯环的羧酸在一定条件下反应生成酯的种类有(不考虑立体异构)( )
| A. | 16种 | B. | 8种 | C. | 12种 | D. | 4种 |
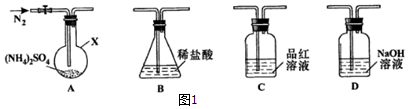
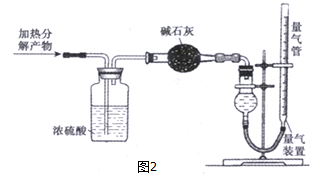

 液褪色
液褪色