题目内容
【题目】近年来,我国机动车保有量持续增长,汽车尾气排放已成为城市的主要污染源,汽车尾气催化净化成为及其重要的环保产业。回答下列问题:
(1)用活性炭还原法可以处理汽车尾气中氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ![]() N2(g)+CO2(g) △H<0。 在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H<0。 在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
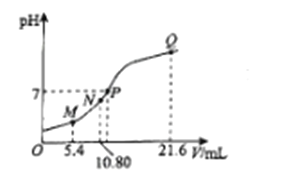
①第一次达平衡时,NO的转化率为_____________ ,T1℃时,该反应的平衡常数K=_______________。
②30min后只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是___________;
③若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol·L-1,则反应达平衡时c(NO)=________。
④若升高温度为T2℃,该反应是平衡常数K减小,原因是_______________。
(2)在汽车排气管加装催化转换器,可有效降低污染物的浓度。已知,催化转换器的效率计算:
ηi= ![]() ×100%。ηi为排气污染物i的催化效率;c1(i)为排气污染物i在入口处的浓度;c2(i)为排气污染物i在出口处的浓度。JPG三元催化剂的部分实验数据如下表:
×100%。ηi为排气污染物i的催化效率;c1(i)为排气污染物i在入口处的浓度;c2(i)为排气污染物i在出口处的浓度。JPG三元催化剂的部分实验数据如下表:
温度/℃ | 流量/(m3·h-1) | CxHy/(106ppm) | CO/% | NOx/(106ppm) | |
入口 | 100 | 0.2 | 139 | 2.66 | 21 |
出口 | 31 | 0 | 0 |
①在上述条件下,η(CO)、η(NOx)均达100%,η(CxHy)=_____________。
②两种不同的催化剂JFG和HPA-8在不同温度、流量下CxHy的去除率如图所示:
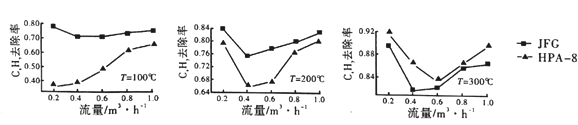
比较两种催化剂在不同温度下对CxHy的转化效率,由此可得出的结论是____________。
【答案】 50% 0.25 缩小容器的体积或通入一定量的NO或通入少量等物质的量的N2、CO2(答出一条即可) 1.25 mol·L-1 该反应为放热反应,故温度升高,平衡常数减小 77.7% 100~200℃,JFG对CxHy的去除率优于HPA-8,300℃时,HPA-8对CxHy的去除率要好于JFG(合理答案均可)
【解析】试题分析:(1)①利用“三段式”计算转化率、平衡常数;②根据影响平衡移动的因素分析;③根据平衡常数不变计算。④若升高温度,该反应是平衡常数K减小,说明平衡逆向移动;(2) ①根据ηi= ![]() ×100%计算;②根据图像分析。
×100%计算;②根据图像分析。
解析:(1)①
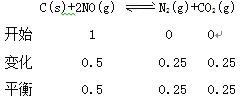
NO的转化率为![]() 50%;平衡常数=
50%;平衡常数=![]()
![]() 0.25;
0.25;
②30min后反应物、生成物浓度都增大,但平衡常数没变,根据影响平衡移动的因素,可能改变的条件是缩小容器的体积或通入一定量的NO或通入少量等物质的量的N2、CO2;③根据平衡常数不变计算
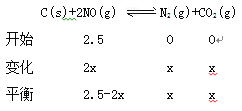
![]() ,x=0.625,反应达平衡时c(NO)=2.5-1.25=1.25 mol·L-1。④若升高温度,该反应是平衡常数K减小,说明平衡逆向移动,所以该反应为放热反应;(2) ①根据ηi=
,x=0.625,反应达平衡时c(NO)=2.5-1.25=1.25 mol·L-1。④若升高温度,该反应是平衡常数K减小,说明平衡逆向移动,所以该反应为放热反应;(2) ①根据ηi= ![]() ×100%=
×100%=![]() 77.7%;②根据图像,100~200℃,JFG对CxHy的去除率优于HPA-8,300℃时,HPA-8对CxHy的去除率要好于JFG。
77.7%;②根据图像,100~200℃,JFG对CxHy的去除率优于HPA-8,300℃时,HPA-8对CxHy的去除率要好于JFG。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 |
S2Cl2+Cl2 2SCl2 |
设计实验装置图如下:

(1)上图中气体发生和尾气处理装置不够完善,请你提出改进意见 。利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式: 。E中反应的化学方程式: 。
(3)C中的试剂是 。
(4)仪器B的名称是 。F的作用是 。
(5)如果在加热E时温度过高,对实验结果的影响是 。
(6)S2Cl2粗品中可能混有的杂质是(填写两种) ,为了提高S2Cl2的纯度,关键的操作是控制好温度和 。