题目内容
有两种金属组成的混合物粉末32g与足量的稀盐酸反应,生成11.2L(标况)H2,则该混合物的组成可能是:①Fe、Zn ②Al、Cu ③Ag、Mg ④Al、Fe
| A.①②③④ | B.①②③ | C.①③ | D.②③④ |
B
试题分析:生成氢气的物质的量=
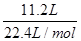 =0.5mol,反应中氢元素的化合价从+1价降低到0价,所以生成0.5mol氢气转移电子的物质的量=0.5mol×2=1.0mol,这说明金属失去1mol电子,消耗金属的质量是32g。Fe、Zn、Al、Mg与盐酸反应时失去1mol电子消耗金属的质量分别是(g)
=0.5mol,反应中氢元素的化合价从+1价降低到0价,所以生成0.5mol氢气转移电子的物质的量=0.5mol×2=1.0mol,这说明金属失去1mol电子,消耗金属的质量是32g。Fe、Zn、Al、Mg与盐酸反应时失去1mol电子消耗金属的质量分别是(g)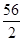 =28、
=28、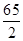 =32.5、
=32.5、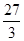 =9、
=9、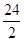 =12,。金属铜和银与盐酸布反应,可以视为无穷大,则根据平均值原理可知组合①Fe、Zn、②Al、Cu、③Ag、Mg均满足,因此答案选B。
=12,。金属铜和银与盐酸布反应,可以视为无穷大,则根据平均值原理可知组合①Fe、Zn、②Al、Cu、③Ag、Mg均满足,因此答案选B。
练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目