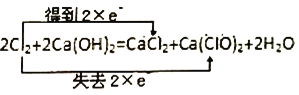题目内容
【题目】下列关于元素化合物的化学用语不正确的是
A.氟离子的结构示意图:![]()
B.H和Cl形成共价键的过程:![]()
C.铅蓄电池放电时的负极反应:Pb(s)+SO42-(aq)-2e-=PbSO4(s)
D.![]() 氧化
氧化![]() 生成单质硫:
生成单质硫:![]()
【答案】B
【解析】
A.氟离子质子数为9,氟离子的最外层含有8个电子,其正确的离子结构示意图为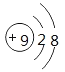 ,故A正确;
,故A正确;
B.氯化氢是共价化合物,无电子的得失,则用电子式表示HCl的形成过程为![]() ,故B错误;
,故B错误;
C.负极发生氧化反应,所以铅蓄电池放电时的负极反应:Pb(s)+SO42-(aq)-2e-=PbSO4(s),故C正确;
D.二氧化硫与硫化氢反应生成单质硫,二氧化硫是氧化剂,硫化氢是还原剂,所以单线表示电子转移方向为:![]() ,故D正确;
,故D正确;
故选B。

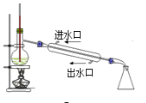
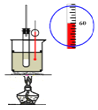
【题目】实验室用50mL 0.50mol/L盐酸、50mL0.55mol/L NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:

实验次数 | 起始温度/℃ | 终止温度/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是___。实验中使用环形玻璃搅拌棒的操作方法是____;
(2)在操作正确的前提下,提高中和热测定准确性的关键是_____;
(3)根据表中所测数据进行计算,则该实验测得的中和热![]() =_____ [盐酸和NaOH溶液的密度按1
=_____ [盐酸和NaOH溶液的密度按1![]() 计算,反应后混合溶液的比热容(c)按4.18
计算,反应后混合溶液的比热容(c)按4.18![]() 计算]。如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的中和热将______ (填“偏大”“偏小”或“不变”)。
计算]。如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的中和热将______ (填“偏大”“偏小”或“不变”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热数值偏低,请你分析可能的原因是__________;
A.测量盐酸的温度后,温度计没有用水冲洗干净 B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 C.做本实验的当天室温较高 D.在量取盐酸时仰视读数 E.大烧杯的盖板中间小孔太大
【题目】(1)据报道,我国在南海进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
二氧化碳重整:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③
则反应①自发进行的条件是___(填“低温”或“高温”),ΔH3=__kJ·mol-1。
(2)根据部分键能数据,以及热化学方程式CH4(g)+4F2(g)=CF4(g)+4HF(g) ΔH=-1940kJ·mol-1,计算H—F键的键能为__kJ·mol-1。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | ? | 155 |
(3)0.1mol的氯气和焦炭、TiO2固体完全反应,生成TiCl4液体和CO气体,放出热量4.28kJ,写出该反应的热化学方程式___。
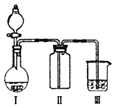
【题目】实验室中某些气体的制取、收集、尾气处理![]() 或性质实验
或性质实验![]() 装置如图所示,用此装置和下表中提供的物质完成相关实验,合理的选项是
装置如图所示,用此装置和下表中提供的物质完成相关实验,合理的选项是![]()
选项 | Ⅰ中的物质 | Ⅱ中收集的气体 | Ⅲ中的物质 |
|
A | Cu和稀硝酸 | NO | NaOH溶液 | |
B | 浓盐酸和 |
| NaOH溶液 | |
C | 亚硫酸钠和浓硫酸 |
| 品红溶液 | |
D | 浓氨水和CaO |
| 酚酞溶液 |
A.AB.BC.CD.D