题目内容
(2008?开封一模)下列离子方程式书写正确的是( )
分析:A.向NaHCO3溶液中滴加过量的Ba(OH)2溶液,碳酸氢根和氢氧根按照物质的量之比是1:1进行反应;
B.过量的SO2通入NaOH溶液中发生2NaOH+SO2═Na2SO3+H2O,Na2SO3+SO2+H2O═2NaHSO3,据此分析解答;
C.方程式左右电荷不守恒;
D.CaCO3是难溶物质应该写化学式;
B.过量的SO2通入NaOH溶液中发生2NaOH+SO2═Na2SO3+H2O,Na2SO3+SO2+H2O═2NaHSO3,据此分析解答;
C.方程式左右电荷不守恒;
D.CaCO3是难溶物质应该写化学式;
解答:解:A.向NaHCO3溶液中滴加过量的Ba(OH)2溶液,碳酸氢根和氢氧根按照物质的量之比是1:1进行反应,即HCO3-+Ba2++OH-═H2O+BaCO3↓,故A错误;
B.过量的SO2通入NaOH溶液中反应生成亚硫酸氢钠,离子反应为:SO2+OH-═HSO3-,故B正确;
C.NaNO2溶液中加入酸性KMnO4溶液,亚硝酸根离子具有还原性,高锰酸根离子具有氧化性,两者发生反应:2MnO4-+5NO2-+6H+═2Mn2++5NO3-+3H2O,故C错误;
D.硝酸酸性强于碳酸,碳酸钙可以和硝酸反应,CaCO3溶解于稀硝酸中离子反应为:CaCO3+2H+═Ca2++H2O+CO2↑,故D错误;
故选:B.
B.过量的SO2通入NaOH溶液中反应生成亚硫酸氢钠,离子反应为:SO2+OH-═HSO3-,故B正确;
C.NaNO2溶液中加入酸性KMnO4溶液,亚硝酸根离子具有还原性,高锰酸根离子具有氧化性,两者发生反应:2MnO4-+5NO2-+6H+═2Mn2++5NO3-+3H2O,故C错误;
D.硝酸酸性强于碳酸,碳酸钙可以和硝酸反应,CaCO3溶解于稀硝酸中离子反应为:CaCO3+2H+═Ca2++H2O+CO2↑,故D错误;
故选:B.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意离子反应中应保留化学式的物质,C中氧化还原反应型的离子反应为该题的难点,题目难度中等.

练习册系列答案
相关题目
 (2008?开封一模)短周期元素的常见单质A、B、C、D在通常状况下均为气态,其中B分子中共价键最多,单质A分别与B、C、D在一定条件下发生反应,得到相应的共价化合物E、F、G,通常状况下F为液体,E、G为气体,且E与G可反应得到离子化合物H,H中的阳离子含有10个电子,阴离子含有18个电子.
(2008?开封一模)短周期元素的常见单质A、B、C、D在通常状况下均为气态,其中B分子中共价键最多,单质A分别与B、C、D在一定条件下发生反应,得到相应的共价化合物E、F、G,通常状况下F为液体,E、G为气体,且E与G可反应得到离子化合物H,H中的阳离子含有10个电子,阴离子含有18个电子.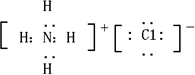

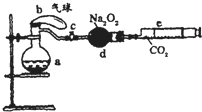 (2008?开封一模)如图所示装置中:a是盛有标准状况下的空气(氧气占
(2008?开封一模)如图所示装置中:a是盛有标准状况下的空气(氧气占