题目内容
15.两种有机化合物A和B互为同分异构体,分子式为C7H8O.A能与氢溴酸反应,生成物的分子式为C7H7Br,而B不能与氢溴酸反应;A不溶于NaOH溶液,而B能溶于NaOH溶液;B能使适量溴水褪色并产生白色沉淀,而A不能.B的一溴代物有三种.(1)写出A、B的结构简式A
 ;B、
;B、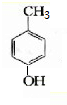 ;
;(2)完成化学方程式:
①B与NaOH溶液:
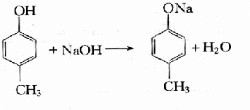
②B与溴水反应:
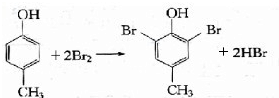 .
.
分析 分子式为C7H8O的有机化合物包括苯甲醇、邻甲基苯酚、间甲基苯酚、对甲基苯酚,能与氢溴酸反应的是苯甲醇,含有酚羟基的物质具有弱酸性,能溶于NaOH溶液,且能使适量溴水退色并产生白色沉淀,故A为苯甲醇,结构简式为 ,邻甲基苯酚的一溴代物有4种、间甲基苯酚的一溴代物有3种、对甲基苯酚的一溴代物有1种,B为对甲基苯酚,结构简式为
,邻甲基苯酚的一溴代物有4种、间甲基苯酚的一溴代物有3种、对甲基苯酚的一溴代物有1种,B为对甲基苯酚,结构简式为 ,据此来书写有机物的结构简式以及化学方程式.
,据此来书写有机物的结构简式以及化学方程式.
解答 解:(1)分子式为C7H8O的有机化合物包括苯甲醇、邻甲基苯酚、间甲基苯酚、对甲基苯酚,能与氢溴酸反应的是苯甲醇,含有酚羟基的物质具有弱酸性,能溶于NaOH溶液,且能使适量溴水退色并产生白色沉淀,故A为苯甲醇,结构简式为 ,邻甲基苯酚的一溴代物有4种、间甲基苯酚的一溴代物有3种、对甲基苯酚的一溴代物有1种,B为对甲基苯酚,结构简式为
,邻甲基苯酚的一溴代物有4种、间甲基苯酚的一溴代物有3种、对甲基苯酚的一溴代物有1种,B为对甲基苯酚,结构简式为 ,
,
故答案为: ;
; ;
;
(2)B为 ,B与NaOH溶液反应的方程式为
,B与NaOH溶液反应的方程式为 ,B与溴水反应的方程式为
,B与溴水反应的方程式为 ,
,
故答案为: ;
; .
.
点评 本题考查学生有机物同分异构体的书写以及有机物的性质,注意知识的梳理和归纳是关键,难度较大.

练习册系列答案
相关题目
5.能正确表示下列反应的离子反应方程式的是( )
| A. | 双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-═I2+2H2O | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-═2 Al(OH)3↓+3BaSO4↓ | |
| C. | 向FeBr2溶液中通入少量氯气:Br-+Cl2═Br2+2Cl- | |
| D. | SO2通入溴水中:SO2+Br2+2H2O═2H++SO42-+HBr |
10.下列有关说法正确的是( )
| A. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| B. | 反应A(g)?2B(g);若正反应的活化能为Ea kJ•mol-1,逆反应的活化能为Eb kJ•mol-1,则该反应的△H=(Ea-Eb)kJ•mol-1 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,平衡时氢气转化率增大 | |
| D. | 吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 |
20.下表为元素周期表的一部分.X、Y、Z、W为短周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍.下列说法正确的是( )
| X | Y | ||
| Z | W | ||
| T |
| A. | X氢化物的沸点一定比Y氢化物的沸点高 | |
| B. | Z的最高价氧化物的水化物酸性一定比W的强 | |
| C. | XZ2、XW4与Na2O的化学键类型相同 | |
| D. | 根据元素周期律,可以推测存在T3Y4、TZ2和TW4 |
4.下列反应的离子方程式不正确的是( )
| A. | 钠和水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 氧化钠与水反应:Na2O+H2O═2Na++2OH- | |
| C. | NaHCO3溶液与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | Na2CO3溶液与BaCl2溶液反应:CO32-+Ba2+═BaCO3↓ |
3. 一定条件下存在反应C(s)+H2O(g)═CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.下列说法正确的是( )
一定条件下存在反应C(s)+H2O(g)═CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.下列说法正确的是( )
 一定条件下存在反应C(s)+H2O(g)═CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.下列说法正确的是( )
一定条件下存在反应C(s)+H2O(g)═CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2molC 1molH2O | 1molCO 1molH2 | 4molC 2molH2O |
| A. | 甲容器中,反应在前15min的平均速率v(H2)=0.1 mol•L-1•min-1 | |
| B. | 丙容器的体积V>0.5L | |
| C. | 当温度为T1℃时,反应的平衡常数K=4.5 | |
| D. | 乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2 |
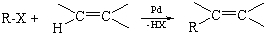
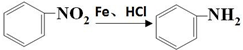

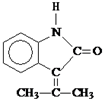 .
.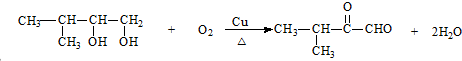 ;F→G:
;F→G: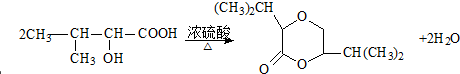 .
.