题目内容
.某化学研究性学习小组对Na2CO3和NaHCO3的混合溶液的组成进行探究。取20.00mL该混合溶液不断加入1.00mol/L的稀盐酸,加入盐酸的体积和产生的现象见下表:

则混合溶液中c(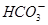 )为
)为

则混合溶液中c(
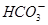 )为
)为| A.0.50mol/L | B.1.00mol/L | C.1.50mol/L | D.2.00mol/L |
B
由表中可知当加入的盐酸为10mL时,没有气体产生,若超过10mL产生了气体说明10mL时发生的反应是溶液中的 转化为
转化为 ,根据盐酸的用量
,根据盐酸的用量 ,可以计算出生成的
,可以计算出生成的 为0.01moL,分析反应Ⅱ和Ⅲ两个阶段可以得到盐酸加入40mL时溶液中的
为0.01moL,分析反应Ⅱ和Ⅲ两个阶段可以得到盐酸加入40mL时溶液中的 完全反应生成了气体,除去前面转化
完全反应生成了气体,除去前面转化 消耗的盐酸,所以与
消耗的盐酸,所以与 反应生成气体的盐酸是30mL,根据方程式可以计算出
反应生成气体的盐酸是30mL,根据方程式可以计算出 的物质的量为
的物质的量为 ,这些
,这些 包含了反应生成的
包含了反应生成的 ,除去这一部分生成的溶液中原有的
,除去这一部分生成的溶液中原有的 为0.03—0.01=0.02moL,浓度为
为0.03—0.01=0.02moL,浓度为 ,答案选B。
,答案选B。
 转化为
转化为 ,根据盐酸的用量
,根据盐酸的用量 ,可以计算出生成的
,可以计算出生成的 为0.01moL,分析反应Ⅱ和Ⅲ两个阶段可以得到盐酸加入40mL时溶液中的
为0.01moL,分析反应Ⅱ和Ⅲ两个阶段可以得到盐酸加入40mL时溶液中的 完全反应生成了气体,除去前面转化
完全反应生成了气体,除去前面转化 消耗的盐酸,所以与
消耗的盐酸,所以与 反应生成气体的盐酸是30mL,根据方程式可以计算出
反应生成气体的盐酸是30mL,根据方程式可以计算出 的物质的量为
的物质的量为 ,这些
,这些 包含了反应生成的
包含了反应生成的 ,除去这一部分生成的溶液中原有的
,除去这一部分生成的溶液中原有的 为0.03—0.01=0.02moL,浓度为
为0.03—0.01=0.02moL,浓度为 ,答案选B。
,答案选B。
练习册系列答案
相关题目