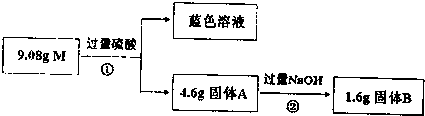
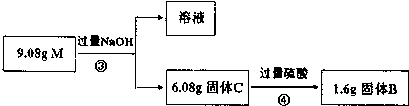
题目内容
19.生活中各种各样的“油”随处可见,下列油属于脂类的是( )| A. | 石油 | B. | 石蜡油 | C. | 甘油 | D. | 菜子油 |
分析 由高级脂肪酸和甘油作用生成的酯为油脂,液态为油,油脂统称为脂类,据此解题.
解答 解:A.石油是多种烃的混合物,故A错误;
B.石蜡油是烃的混合物,故B错误;
C.甘油是丙三醇,故C错误;
D.菜子油是主要成分是油脂,属于脂类,故D正确.
故选D.
点评 本题考查脂质的种类,难度不大,只要考生识记相关知识点即可正确答题,属于考纲识记层次的考查,此类试题,需要考生掌握牢固的基础知识.

练习册系列答案
相关题目
9.下列各种装置属于原电池的是( )
| A. |  稀硫酸 | B. |  稀硫酸 | C. | 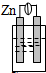 酒精 | D. | 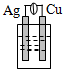 稀硫酸 |
10.四种短周期元素在周期表中的位置如右图,其中只有M为金属元素,下列说法错误的是( )

| A. | Y的气态氢化物与其最高价氧化物水化物能反应生成盐 | |
| B. | X的单质可做半导体和光电纤维材料 | |
| C. | M和Y的最高价氧化物对应水化物之间能相互反应 | |
| D. | Z的气态氢化物比Y的气态氢化物稳定 |
14.常温下,下列各组物质因存在氧化还原反应而不能共存的是( )
| A. | H+,C6H5O-,CH3COO-,MnO4- | B. | 葡萄糖,Cu2+,Na+,OH- | ||
| C. | Fe3+,NO3-,SO42-,H+ | D. | OH-,Al3+,NH4+,AlO2- |
4.已知I-、Fe2+、SO2、Cl-、H2O2在酸性溶液中的还原性强弱顺序为:SO2>I->H2O2>Fe2+>Cl-,试判断下列反应不可能发生的是( )
| A. | H2O2+SO2═H2SO4 | B. | I2+2Fe2+═2I+2Fe3+ | ||
| C. | 2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | D. | SO2+2H2O+I2═H2SO4+2HI |
11.下列物成中,互为同分异构体的是( )
| A. | 淀粉和纤维素 | B. | 淀粉和葡萄糖 | C. | 蔗糖和麦芽糖 | D. | 果糖和蔗糖 |
8.如图立方烷(C8H8)的球棍模型,下列有关说法不正确的是( )
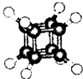

| A. | 它的一氯代物只有一种同分异构体 | |
| B. | 它的二氯代物有三种同分异构体 | |
| C. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 | |
| D. | 它是一种不饱和烃,既能发生取代反应,又能发生加成反应 |
3.(1)在1200℃时,天然气脱硫工艺中会发生下列反应:
①H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)═S(g)+H2O(g)△H3
④2S(g)═S2(g)△H4
则△H4的正确表达式为$\frac{2}{3}$(△H1+△H2-3△H3).
(2)某可逆反应:X(g)+3Y(g)?2Z(g)平衡常数与温度关系如表所示:
①根据上述数据判断,该可逆反应的正反应是放热(填“吸热”或“放热”)反应,理由是温度升高,平衡常数减小.
②为了增大X的转化率和反应速率,宜采用的措施是B.
A.升高温度 B.增大压强 C.加催化剂 D.分离Z
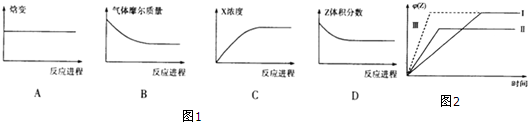
③在2L密闭容器中充入Z气体,在一定条件下进行反应.下列图1象不能表明该反应达到平衡状态的是A.
④440℃时,在2L密闭容器中,开始充入1mol X气体和3mol Y气体进行反应.在某时刻测得c(X)=0.45mol/L,此时,反应是否达到平衡状态否(填“是”或“否”),简述理由:此时浓度商Q=$\frac{{c}^{2}(Z)}{c(X){c}^{3}(Y)}$=$\frac{0.{1}^{2}}{0.45×1.3{5}^{3}}$=0.0090<K,平衡正向进行.
⑤在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图2所示(曲线I为标准):
ⅰ曲线Ⅱ改变的条件是升温.
ⅱ曲线Ⅲ改变的条件是加合适的催化剂.
①H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)═S(g)+H2O(g)△H3
④2S(g)═S2(g)△H4
则△H4的正确表达式为$\frac{2}{3}$(△H1+△H2-3△H3).
(2)某可逆反应:X(g)+3Y(g)?2Z(g)平衡常数与温度关系如表所示:
| 温度/℃ | 360 | 440 | 520 |
| K | 0.036 | 0.010 | 0.0038 |
②为了增大X的转化率和反应速率,宜采用的措施是B.
A.升高温度 B.增大压强 C.加催化剂 D.分离Z
③在2L密闭容器中充入Z气体,在一定条件下进行反应.下列图1象不能表明该反应达到平衡状态的是A.

④440℃时,在2L密闭容器中,开始充入1mol X气体和3mol Y气体进行反应.在某时刻测得c(X)=0.45mol/L,此时,反应是否达到平衡状态否(填“是”或“否”),简述理由:此时浓度商Q=$\frac{{c}^{2}(Z)}{c(X){c}^{3}(Y)}$=$\frac{0.{1}^{2}}{0.45×1.3{5}^{3}}$=0.0090<K,平衡正向进行.
⑤在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图2所示(曲线I为标准):
ⅰ曲线Ⅱ改变的条件是升温.
ⅱ曲线Ⅲ改变的条件是加合适的催化剂.