题目内容
【题目】下列说法正确的是( )
A.在纯水中加入盐一定促进水的电离
B.同温时,等浓度的NaHCO3和Na2CO3溶液,NaHCO3溶液的pH大
C.加热CH3COONa溶液,溶液中![]() 的值将变大
的值将变大
D.0.1mol·L-1HA弱酸溶液与0.05mol·L-1NaOH溶液等体积混合,所得溶液中:2c(H+)+c(HA)=c(A-)+2c(OH-)
【答案】D
【解析】
A.在纯水中加入能够水解的盐才会促进水的电离,A选项错误;
B.同温度时,CO32-的水解程度大于HCO3-,因此Na2CO3溶液的碱性强,pH大,B选项错误;
C.加热CH3COONa溶液,CH3COO-的水解程度增大,c(CH3COO-)减小,c(Na+)不变,则![]() 的值减小,C选项错误;
的值减小,C选项错误;
D.0.1mol·L-1HA弱酸溶液与0.05mol·L-1NaOH溶液等体积混合,所得溶液为等浓度的NaA和HA的混合溶液,根据电荷守恒可以知道c(H+)+c(Na+)=c(A-)+c(OH-),根据物料守恒可以知道2c(Na+)=c(HA)+c(A-),两式联立可得2c(H+)+c(HA)=c(A-)+2c(OH-),D选项正确;
答案选D。

【题目】运用所学知识回答下列问题:
(1)常温下实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:___。
(2)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2(s) ΔH=-989.2kJ·mol-1,有关键能数据如下表:
化学键 | Si—O | O=O | Si—Si |
键能/kJ·mol-1 | x | 498.8 | 176 |
已知1molSi中含2molSi—Si键,1molSiO2中含4molSi—O键,则x的值为__。
(3)AgNO3的水溶液呈___(填“酸”、“中”、“碱”)性,实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,目的是___。
(4)在稀释醋酸的过程中,下列始终保持增大趋势的量是(______)
A.c(H+) B.H+个数 C.CH3COOH分子数 D.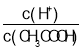
(5)某温度(t℃)时,水的离子积为Kw=1×10-13。若将此温度下pH=11的苛性钠溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),若所得混合溶液的pH=2,则a∶b=__。
(6)已知Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应至少调至__。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应至少调至__。