题目内容
(13分)氢气是一种清洁能源,可以通过多种方法制得。
(1) 工业上用水煤气法制氢气,有关化学方程式是:
反应一:C( s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g) △H> 0
CO(g) + H2(g) △H> 0
反应二:CO(g) + H2O(g) CO2(g) + H2(g) △H < 0
CO2(g) + H2(g) △H < 0
①若反应一在t℃时达到化学平衡状态,则此温度下该反应的的平衡常数表达式
K = ;
②在427℃时将CO 和H2O(g)各0.01mol通入体积为2升的密闭容器中反应,5分钟时达到平衡状态,该反应的平衡常数是9,则CO的转化率是 ,用CO的浓度变化表示的反应率速v(CO)是 mol /(L·min)。
(2)利用电解饱和食盐水也可制得氢气,下图为电解食盐水的示意图:

请回答:
① C1电极是 极(填“阴”或“阳”),C2电极的电极反应式是 。
②该电解反应的离子方程式是 ,
(3)通过下列方法也可以得到氢气。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ·mol-1
1molCH4(g)与H2O(g)反应生成CO2(g)和H2(g)的反应热是 kJ·mol-1。
(1) 工业上用水煤气法制氢气,有关化学方程式是:
反应一:C(
 s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g) △H> 0
CO(g) + H2(g) △H> 0 反应二:CO(g) + H2O(g)
 CO2(g) + H2(g) △H < 0
CO2(g) + H2(g) △H < 0①若反应一在t℃时达到化学平衡状态,则此温度下该反应的的平衡常数表达式
K = ;
②在427℃时将CO 和H2O(g)各0.01mol通入体积为2升的密闭容器中反应,5分钟时达到平衡状态,该反应的平衡常数是9,则CO的转化率是 ,用CO的浓度变化表示的反应率速v(CO)是 mol /(L·min)。
(2)利用电解饱和食盐水也可制得氢气,下图为电解食盐水的示意图:

请回答:
① C1电极是 极(填“阴”或“阳”),C2电极的电极反应式是 。
②该电解反应的离子方程式是 ,
(3)通过下列方法也可以得到氢气。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ·mol-1
1molCH4(g)与H2O(g)反应生成CO2(g)和H2(g)的反应热是 kJ·mol-1。
(13分)
(1)①K =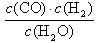
② 0.75 或 75% 、 7.5×10-4
(2)①阳、 2H+ + 2 e- = H2↑
② 2Cl- + 2H2O Cl2↑ + H2↑ + 2OH-
Cl2↑ + H2↑ + 2OH-
(3)+ 659.8
(1)①K =
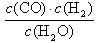
② 0.75 或 75% 、 7.5×10-4
(2)①阳、 2H+ + 2 e- = H2↑
② 2Cl- + 2H2O
 Cl2↑ + H2↑ + 2OH-
Cl2↑ + H2↑ + 2OH-(3)+ 659.8
略

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案
相关题目
 C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0 (填“>”、“<”、“无法确定”)。
C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0 (填“>”、“<”、“无法确定”)。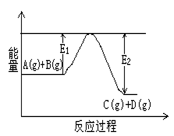
 O的热化学方程式为 。
O的热化学方程式为 。 化剂液态双氧水(H2O2)。
化剂液态双氧水(H2O2)。 存在;
存在; 2C(g) △H=QkJ·mol-1(Q<0)
2C(g) △H=QkJ·mol-1(Q<0)
 列说法或表示方法中正确的是( )
列说法或表示方法中正确的是( )

 H
H )和强氧化剂H
)和强氧化剂H