题目内容
【题目】同一周期的X、Y、Z三种元素,已知它们最高价氧化物对应水化物的酸性强弱是H3XO4<H2YO4<HZO4,下列推断不正确的是( )
A. 原子序数:X<Y<Z B. 气态氢化物稳定性:XH3<H2Y<HZ
C. 元素的非金属性强弱:X>Y>Z D. 最外层电子数:Z>Y>X
【答案】C
【解析】非金属性越强,相应最高价氧化物的水化物的酸性就越强。同周期元素自左向右原子半径逐渐增大,金属性逐渐减弱,非金属性逐渐增强,根据最高价含氧酸的酸性强弱顺序可知非金属性是X<Y<Z ,所以原子序数是X<Y<Z ,最外层电子数是X<Y<Z。非金属性越强,氢化物的稳定性就越强,所以气态氢化物稳定性:XH3<H2Y<HZ。答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
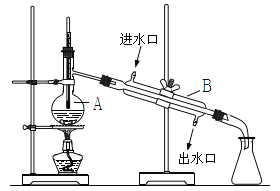
【题目】某化学兴趣小组利用下图装置进行乙酸乙酯合成和分离的实验探究,请回答以下问题

(1)写出合成乙酸乙酯的化学方程式_______________________________。
(2)仪器b的名称________,图中起冷凝回流作用的是______(填a、b、c、d、e)。
(3)为了提高乙酸乙酯的产率可采取的措施 _______________________________
(4)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏。
物质 | 98.3%浓硫酸 | 乙酸乙酯 | 乙酸 | 乙醇 | 乙醚 | 水 |
沸点 | 338℃, | 77.1℃ | 118℃ | 78.5℃ | 34.6℃ | 100℃ |
根据上表分析,蒸馏后得到的乙酸乙酯中,最有可能含有________________杂质。