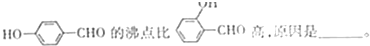
题目内容
9.下列说法正确的是( )| A. | P和S属于第三周期元素,P的第一电离能比S小 | |
| B. | Na和Rb属于第ⅠA族元素,Rb失电子能力比Na强 | |
| C. | C和Si属于第ⅣA族元素,Si比C更容易和氢气反应 | |
| D. | Cl和Br属于第ⅦA族元素,HClO4酸性比HBrO4弱 |
分析 A、同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族和第VA族元素第一电离能大于其相邻元素;
B、同主族从上到下失电子能力逐渐增强;
C、同主族自上而下非金属性减弱,非金属性越强,与氢气反应更容易;
D、同主族自上而下非金属性减弱,非金属性越强,最高价含氧酸的酸性越强.
解答 解:A.同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族和第VA族元素第一电离能大于其相邻元素,所以P元素第一电离能大于S元素,故A错误;
B、同主族从上到下失电子能力逐渐增强,Na和Rb属于第ⅠA族元素,则Rb失电子能力比Na强,故B正确;
C、C和Si属于第ⅣA族元素,同主族自上而下非金属性减弱,故C比Si更容易和氢气反应,故C错误;
D、Cl和Br属于第ⅦA族元素,同主族自上而下非金属性减弱,非金属性越强,最高价含氧酸的酸性越强,故D错误.
故选B.
点评 本题考查了元素周期律的应用,明确同周期和同主族元素性质的递变规律即可解答,题目难度不大.

练习册系列答案
相关题目
20.硝酸的化学性质
(1)实验探究,观察与思考,硝酸的性质实验
(2)请写出Cu与浓,稀HNO3反应的化学反应方程式
(1)实验探究,观察与思考,硝酸的性质实验
| 实验装置 | 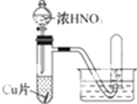 |  |
| 实验现象 | a.Cu片溶解溶液变成篮色. b.溶液中有气泡产生,大使管中充满红棕色气体气体,小试管中为无色气体 c、反应剧烈 | a、Cu片溶解,溶液变成蓝色. b.溶液中有气泡产生,大试管、小试管中均为无色气体 c.反应不剧烈 |
| 实验结论 | 浓硝酸具有氧化性,还原产物为NO2 | 稀硝酸具有氧化性,但不如浓硝酸强,还原产物为NO |

17.下列离子方程式中书写正确的是( )
| A. | Al2O3与NaOH溶液反应 Al2O3+2OH-═2 AlO2-+H2O | |
| B. | FeCl2溶液中通入Cl2 Fe2++Cl2═Fe3++2Cl- | |
| C. | FeCl3溶液与铜 Fe3++Cu═Fe2++Cu2+ | |
| D. | 用醋酸除水垢 2H++CaCO3═Ca2++H2O+CO2↑ |
14.下列有关乙醇的说法中,不正确的是( )
| A. | 属于烃类物质 | B. | 相对分子质量为46 | ||
| C. | 分子中含有的官能团是羟基 | D. | 在空气中完全燃烧生成CO2和H2O |
1.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH21,3-二丁烯 | B. | 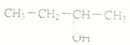 3-丁醇 | ||
| C. | 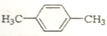 二甲苯 | D. | 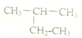 2-甲基丁烷 2-甲基丁烷 |
18.下列电离方程式中不正确的是( )
| A. | H2SO4═2H++SO42- | B. | Ba(OH)2═Ba2++2OH- | ||
| C. | NaNO3═Na++NO3- | D. | KClO3═K++Cl-+3O2- |
19.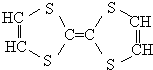 用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
 用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )| A. | 分子中含有碳碳双键,属于烯烃 | |
| B. | 从碳骨架形状分析,应该属于环状烃 | |
| C. | 该分子属于高分子化合物 | |
| D. | 该分子中即有极性键,也有非极性键 |