题目内容
【题目】对于平衡体系:mA(g)+ nB(g)![]() pC(g)+ qD(g),下列判断正确的是( )
pC(g)+ qD(g),下列判断正确的是( )
A.若温度不变将容器的容积增大1倍,达到新平衡时A的浓度变为原来的0.55 倍,则m+n<p+q
B.若升高平衡体系的温度,达到新平衡时A 的浓度变为原来的0.55 倍,说明该反应△ H<0
C.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
D.若平衡后同时增大A、B的浓度,则A、B的转化率一定都减小
【答案】C
【解析】
试题分析:A、若温度不变,将容器的容积增大1倍,达到新平衡时A的浓度为原来的0.55倍,说明平衡逆向进行,逆向是气体体积增大的反应,m+n>p+q,故A错误;B.若升高平衡体系的温度,达到新平衡时A 的浓度变为原来的0.55 倍,说明平衡正向移动,说明正反应是吸热反应,△H>0,故B错误;C、若平衡时,A、B的转化率相等,转化率是转化量除以起始量计算,说明反应开始时,A、B的物质的量之比为m:n,故C正确;D.若平衡后同时增大A、B的浓度,若与原平衡等效,转化率不变,否则转化率可能增大,可能减小,可能1个增大,1个减小,故D错误;故选C。

【题目】某温度时,在一个容积为2 L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
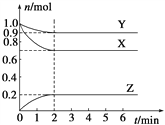
(1)该反应的化学方程式为_______________。
(2)反应开始至2 min,气体Z的反应速率为____________。
(3)若X、Y、Z均为气体,反应达到平衡时,压强是开始时的________倍;此时放出了a kJ的热量,则按(1)的反应方程式写成热化学反应方程式时,该反应的反应热ΔH=_____________。
(4)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。已知:
化学键 | H—H | H—Cl | Cl—Cl |
键能/ kJ·mol–1 | 436 | 431 | 242 |
工业上通过氢气在氯气中充分燃烧制取HCl气体,写出该反应的热化学反应方程式:_______________。


