题目内容
【题目】短周期主族元素![]() 、
、![]() 、
、![]() 、
、![]() 的原子序数依次增大,
的原子序数依次增大,![]() 的最高正价与最低负价代数和为0,
的最高正价与最低负价代数和为0,![]() 、
、![]() 、
、![]() 形成的化合物甲的结构如图所示,
形成的化合物甲的结构如图所示,![]() 在同周期中原子半径最小。下列说法正确的是( )
在同周期中原子半径最小。下列说法正确的是( )
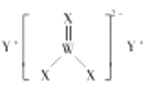
A.原子半径大小:![]()
B.电负性大小:![]()
C.![]() 、
、![]() 形成的化合物为离子化合物
形成的化合物为离子化合物
D.化合物甲中阴离子的空间构型为三角锥形
【答案】AC
【解析】
短周期主族元素W、X、Y、Z的原子序数依次增大,W的最高正价与最低负价代数和为0,则W为C或Si,根据W、X、Y形成的化合物甲的结构示意图,X为O,则W为C,Y为+1价的阳离子,为Na元素;Z在同周期中原子半径最小,Z为Cl元素,据此分析解答。
根据上述分析,W为C元素,X为O元素,Y为Na元素,Z为Cl元素。
A.同一周期,从左到右,原子半径逐渐减小,同一主族,从上到下,原子半径逐渐增大,原子半径大小:![]() ,故A正确;
,故A正确;
B.元素的非金属性越强,电负性越大,电负性大小:X>Z,故B错误;
C.X为O元素,Y为Na元素,为活泼的非金属和金属元素,形成的化合物为离子化合物,故C正确;
D.化合物甲中阴离子为CO32-,C原子的价层电子对数=3,没有孤对电子,空间构型为平面三角形,故D错误;
故选AC。

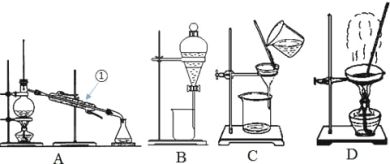
【题目】某实验小组设计用50 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1氢氧化钠溶液在如图装置中进行中和反应。试回答下列问题:
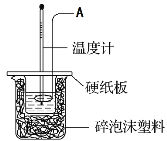
(1)仪器A的名称__________________________
(2)实验过程中下列操作正确是______________(填字母)。
A.用温度计小心搅拌
B.分多次加入氢氧化钠溶液
C.只进行一次实验,用所获得的数据计算中和热
D.用套在温度计上的A轻轻地上下搅动
(3)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__________ (结果保留一位小数)。
(4)以下操作,会使测得的中和热ΔH发生怎样的变化?(填“偏大”“偏小”或“不变”)。
①量取稀盐酸时俯视量筒读数,测得的中和热ΔH会_______________ 。
②在中和热测定实验中未用水洗涤温度计上的盐酸直接测定碱的温度,测得的中和热ΔH会_______________。
③若用等浓度的醋酸与 NaOH 溶液反应,则测得的中和热ΔH会 __________,其原因是____________________________________________________________________________。
【题目】Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素 | 相关信息 |
Y | 原子核外有6个不同运动状态的电子 |
Z | 非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同 |
W | 主族元素,与Z原子的价电子数相同 |
R | 价层电子排布式为3d64s2 |
M | 位于第ⅠB族,其被称作“电器工业的主角” |
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是____,M2+的核外电子排布式为_______。
(2)M2Z的熔点比M2W的______(填“高”或“低”),请解释原因:_____________。
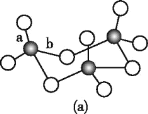
(3)WZ2的VSEPR模型名称为______;WZ3气态为单分子,该分子中W原子的杂化轨道类型为____;WZ3的三聚体环状结构如图(a)所示,该结构的分子中含有____个σ键;写出一种与WZ3互为等电子体的分子的化学式_____。
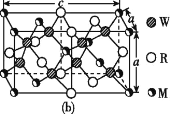
(4)MRW2的晶胞如图(b)所示,晶胞参数a=0.524 nm、c=1.032 nm;MRW2的晶胞中,晶体密度ρ=____g/cm3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA=6.02×1023 mol-1)。