题目内容
【题目】某小组同学用一种铝铁合金为原料,模拟相关的工业生产,反应过程如图所示(部分产物和条件已略去),请回答:
(1)铁铝合金是一种高电磁性能合金,下列有关推测可能正确的是_____(填序号).
A.铁铝合金可由铁和铝熔融混合制成
B.铁铝合金的熔点高于铝和铁
C.铁铝合金硬度高于纯铝
(2)反应①中铝元素发生反应的离子方程式为 .
(3)反应②的化学方程式为 .
(4)反应③发生时观察到的现象是 .
(5)反应④中的CO2不宜换成HCl,原因是 .
(6)请分别举出固体A和B的一种用途、 .
【答案】
(1)A,C
(2)Al3++4OH﹣=AlO2﹣+2H2O
(3)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(4)先产生白色沉淀,之后迅速变成灰绿色最后变为红褐色
(5)过量的氯化氢会使生成的氢氧化铝溶解
(6)做红色油漆,冶炼铝
【解析】解析:(1)根据以上分析,铁铝合金可由铁和铝熔融混合制成,故A正确;铁铝合金的熔点低于铝和铁,故B错误;铁铝合金硬度高于纯铝,故C正确;(2)反应① 是硫酸铝与过量氢氧化钠生成偏铝酸钠和硫酸钠,离子方程式为Al3++4OH﹣=AlO2﹣+2H2O;(3)反应②是铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑;(4)反应③ 是硫酸亚铁与氢氧化钠溶液反应生成白色氢氧化亚铁沉淀和硫酸钠,氢氧化亚铁易被氧气氧化成红褐色氢氧化铁,现象是先产生白色沉淀,之后迅速变成灰绿色最后变为红褐色;(5)偏铝酸钠与过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,偏铝酸钠与过量HCl反应生成氯化铝,所以反应④中的CO2不宜换成HCl;(6)固体A是氧化铁,可做红色油漆;固体B是氧化铝,可以用来冶炼铝;
铁只溶于硫酸,铝既溶于盐酸转变成铝盐,也会溶于氢氧化钠,转变成偏铝酸盐
故1、与氢氧化钠反应后的固体是铁,遇硫酸生成硫酸亚铁,遇氢氧化钠转变成氢氧化亚铁,在空气中被氧气氧化成氢氧化铁
故2、铁溶于硫酸转变成硫酸亚铁,铝溶于盐酸转变成铝盐,遇过量氢氧化钠,硫酸亚铁转变成氢氧化亚铁沉淀,硫酸铝与过量氢氧化钠生成偏铝酸钠和硫酸钠溶液:(沉淀最终转化成固体氢氧化铁,灼烧转化成氧化铁;溶液中NaAlO2与过量二氧化碳反应生成氢氧化铝沉淀,灼烧转化成氧化铝)
(1)合金特点:比组成金属的熔点低、硬度高
(2)反应① 是硫酸铝与过量氢氧化钠生成偏铝酸钠和硫酸钠,离子方程式为Al3++4OH﹣=AlO2﹣+2H2O
(3)反应②是铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(4)反应③ 是硫酸亚铁与氢氧化钠溶液反应生成白色氢氧化亚铁沉淀和硫酸钠,氢氧化亚铁易被氧气氧化成红褐色氢氧化铁,现象是先产生白色沉淀,之后迅速变成灰绿色最后变为红褐色
(5)偏铝酸钠与过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,偏铝酸钠与过量HCl反应生成氯化铝,所以反应④中的CO2不宜换成HCl
(6)固体A是氧化铁,可做红色油漆;固体B是氧化铝,可以用来冶炼铝

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】Q、R、T、X、Y、Z是六种原子序数依次增大的前四周期常见元素,其相关信息如表:
元素 | 相关信息 |
Q | Q的单质是实验室常用的惰性电极材料 |
R | R原子基态时2p原子轨道上有3个未成对电子 |
T | 负二价的元素T的氢化物在通常情况下是一种液体,且 T的质量分数为88.9% |
X | X是第三周期电负性最大的元素 |
Y | 元素Y位于周期表第10列 |
Z | Z存在质量数为65,中子数为36的核素 |
(1)Z元素的原子基态时的电子排布式是
(2)下列叙述正确的是 a.Q的最简单气态氢化物比R的气体氢化物稳定
b.Q的含氧酸一定比R的含氧酸酸性强
c.R的气态氢化物的熔点在同族元素形成的氢化物中最低
d.R的第一电离能、电负性都比Q大
(3)Q和T可形成两种常见化合物,分别表示为QT与QT2 . QT分子中σ键π键的个数比为;QT2分子中,Q原子采取杂化.
(4)笑气(R2T)是一种麻醉剂,有关理论认为R2T与QT2具有相似的结构.故的空间构型为 , 且为(填“极性”或“非极性”)分子.
(5)现有Q、Y和镁三种元素的某种晶体具有超导性,其晶胞结构如图所示.该晶体的化学式为;晶体中每个镁原子周围距离相等且最近的Y原子有个. 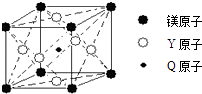
【题目】汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.德国大众汽车尾气检测造假事件引起全世界震惊.根据下列示意图回答有关问题: 
(1)汽车发动机工作时会引发N2(g)+O2(g)=2NO(g)△H=+180kJmol﹣1 , 其能量变化示意图如下: ![]()
则NO中氮氧键的键能为kJmol﹣1;
(2)空燃比过小易产生CO.有人提出可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染.判断该设想是否可行,并说出理由;
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)N2(g)+xCO2 (g)△H=﹣b kJmol﹣1 . 若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是;
A.增加排气管长度
B.增大尾气排放口
C.升高排气管温度
D.添加合适的催化剂
(4)催化装置中涉及的反应之一为:2NO(g)+2CO(g)N2(g)+2CO2(g). 
①探究上述反应中NO的平衡转化率与压强、温度的关系,得到图2所示的曲线.催化装置比较适合的温度和压强是;
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图3所示.则前10s 内,CO和NO百分含量没明显变化的原因是;
③研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
实验编号 | T(K) | NO初始浓度 | CO初始浓度 | 催化剂的比表面积(m2/g) |
Ⅰ | 400 | 1.00×10﹣3 | 3.60×10﹣3 | 82 |
Ⅱ | 400 | 1.00×10﹣3 | 3.60×10﹣3 | 124 |
Ⅲ | 450 | 1.00×10﹣3 | 3.60×10﹣3 | 124 |
根据坐标图4,计算400K时该反应的平衡常数为 .