题目内容
5.下列关于胶体的说法中不正确的是( )| A. | 可以通过过滤的方法将淀粉胶体中混有的氯化钠溶液除去 | |
| B. | 分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| C. | 一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路 | |
| D. | 制备Fe(OH)3胶体的方法是将饱和FeCl3溶液滴加到沸水中煮沸至溶液呈红褐色 |
分析 A、胶体和溶液都能透过滤纸;
B、根据分散系中分散质粒子的大小分析;
C、根据胶体具有丁达尔现象的性质分析;
D、加热条件下三氯化铁水解生成氢氧化铁胶体;
解答 解:A、胶体和溶液都能透过滤纸,所以不能通过过滤的方法将淀粉胶体中混有的氯化钠溶液除去,故A错误;
B、根据分散系中分散质粒子的大小把分散系分为:浊液(>100nm)、胶体(1~100nm)、溶液(<1nm),所以分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)胶体>FeCl3溶液,故B正确.
C、蛋白质溶液属于胶体,能产生丁达尔效益,所以一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路,故C正确;
D、加热条件下三氯化铁水解生成氢氧化铁胶体,则制备Fe(OH)胶体的方法是将饱和FeCl3溶液滴加到沸水中煮沸至溶液呈红褐色,故D正确;
故选A.
点评 本题考查了分散系分类的依据,胶体的性质,胶体的制备等,题目比较简单.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
13.少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率可以使用如下方法( )
| A. | 加H2O | B. | 滴入几滴浓盐酸 | ||
| C. | 增大压强 | D. | 升高温度(不考虑盐酸挥发) |
20.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 4.48L F2变为离子时,获得的电子数为0.2NA | |
| B. | 16g甲烷所含的原子数为NA | |
| C. | 2molNa与足量的O2反应无论是生成Na2O还是Na2O2时电子转移数目为2NA | |
| D. | 18g重水(D2O)所含的电子数为10NA |
10.下列按纯净物、混合物、电解质、非电解质顺序排列的是( )
| A. | 盐酸、空气、醋酸、干冰 | B. | 冰醋酸、碱石灰、硫酸钠、乙醇 | ||
| C. | 蛋白质、油脂、苛性钠、石灰石 | D. | 胆矾、漂白粉、氯化钾、硫酸钡 |
17.下列说法错误的是( )
| A. | 铍(Be)的原子失去电子能力比镁弱 | |
| B. | 砹(At)的氢化物不稳定 | |
| C. | 硫化氢比硒(Se)化氢稳定 | |
| D. | 氢氧化锶[Sr(OH)2]比氢氧化钙的碱性弱 |
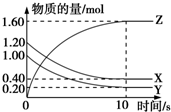 (1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
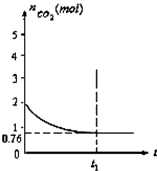 一定温度下2L的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应:
一定温度下2L的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应: