题目内容
将等物质的量A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,且c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L?min).求:
(1)反应开始前放入容器中A、B物质的量.
(2)B的平均反应速率.
(3)x值是多少?
(1)反应开始前放入容器中A、B物质的量.
(2)B的平均反应速率.
(3)x值是多少?
分析:(1)根据D的浓度求出D的物质的量,结合方程式求出A、B的物质的量;
(2)先求出反应的B的物质的量,再根据平均反应速率公式计算B的平均反应速率;
(3)根据同一反应中反应速率之比等于化学计量数之比求出x值.
(2)先求出反应的B的物质的量,再根据平均反应速率公式计算B的平均反应速率;
(3)根据同一反应中反应速率之比等于化学计量数之比求出x值.
解答:解:(1)5分钟后,n(D)=CV=0.5mol/L×2L=1mol,设反应开始前放入容器中A、B物质的量为mmol,
3A(g)+B(g)?xC(g)+2D(g),
反应前 m mol m mol 0 0
5分钟后 ( m-1.5)mol ( m-0.5)mol 1mol
c(A):c(B)=3:5=( m-1.5)mol:( m-0.5)mol
m=3 mol
答:反应开始前放入容器中A、B物质的量均为3mol;
(2)设反应 的B的物质的量为nmol,
3A(g)+B(g)?xC(g)+2D(g),
1 2
nmol 1mol
n=0.5
根据v(B)=
=
=0.05 mol/(L.min)
答:B的平均反应速率为0.05 mol/(L.min);
(3)根据同一反应中反应速率之比等于化学计量数之比,所以v(B):v(C)=0.05 mol/(L.min):0.1mol/(L?min)=1:x,所以x=2.
答:x值是2.
3A(g)+B(g)?xC(g)+2D(g),
反应前 m mol m mol 0 0
5分钟后 ( m-1.5)mol ( m-0.5)mol 1mol
c(A):c(B)=3:5=( m-1.5)mol:( m-0.5)mol
m=3 mol
答:反应开始前放入容器中A、B物质的量均为3mol;
(2)设反应 的B的物质的量为nmol,
3A(g)+B(g)?xC(g)+2D(g),
1 2
nmol 1mol
n=0.5
根据v(B)=
| △n |
| V×△t |
| 0.5mol |
| 2L×5min |
答:B的平均反应速率为0.05 mol/(L.min);
(3)根据同一反应中反应速率之比等于化学计量数之比,所以v(B):v(C)=0.05 mol/(L.min):0.1mol/(L?min)=1:x,所以x=2.
答:x值是2.
点评:本题考查了化学反应速率与化学计量数的关系,明确同一反应中反应速率之比等于化学计量数之比是解(3)的关键.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
 cC(固)+dD当反应进行一定时间后,测得A减少了n
mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n
mol,此时达到化学平衡:
cC(固)+dD当反应进行一定时间后,测得A减少了n
mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n
mol,此时达到化学平衡: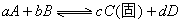 当反应进行一定时间后,测得A减少了n mol,B减少了n/2mol,C增加了3n/2mol,D增加了n mol,此时达到化学平衡:
当反应进行一定时间后,测得A减少了n mol,B减少了n/2mol,C增加了3n/2mol,D增加了n mol,此时达到化学平衡: