题目内容
一定体积0.01 mol·L-1的稀硝酸恰好能氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO。若用0.01 mol·L-1 NaOH溶液溶解相同质量的该混合物,当反应完全时所需氢氧化钠溶液的体积是稀硝酸的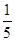 ,则样品中铁、铝的物质的量之比为( )。
,则样品中铁、铝的物质的量之比为( )。
| A.2∶3 | B.1∶3 | C.1∶4 | D.5∶3 |
C
解析

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
从南方往北方长途运输水果时,常常将浸泡有酸性高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是
| A.利用酸性高锰酸钾溶液杀死水果周围的细菌,防止水果霉变 |
| B.利用酸性高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂 |
| C.利用酸性高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟 |
| D.利用酸性高锰酸钾溶液的氧化性,催熟水果 |
已知下列反应:Co2O3 + 6HCl(浓) = 2CoCl2 + Cl2↑+ 3H2O (I)
5Cl2 + I2 + 6H2O =" 10HCl" + 2HIO3 (II)
下列说法正确的是
| A.反应I中HCl是氧化剂 |
| B.反应II 中Cl2发生氧化反应 |
| C.还原性:CoCl2> HCl > I2 |
| D.氧化性:Co2O3> Cl2>HIO3 |
铁粉和铜粉的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9.6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | V |
下列计算结果正确的是 ( )
A.①中溶解了5.6gFe B.硝酸的浓度为0.4mol/L
C.②中溶解了9.6gCu D.④中V=8960
下列物质与水反应不属于氧化还原反应的是
| A.NO2 | B.CaO | C.Cl2 | D.Na2O2 |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是
A.原混合酸中 物质的量浓度为2 mol/L 物质的量浓度为2 mol/L |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol/L |
火法炼铜首先要焙烧黄铜矿,其反应为2CuFeS2+O2—→Cu2S+2FeS+SO2下列说法正确的是
| A.SO2既是氧化产物又是还原产物 |
| B.CuFeS2仅作还原剂,硫元素被氧化 |
| C.每生成1 mol Cu2S,有4 mol硫被氧化 |
| D.每转移1.2 mol电子,有0.2 mol硫被还原 |
氢化亚铜(CuH)是一种不稳定的物质,能在氯气中燃烧,也能与酸反应。用CuSO4溶液和“某物质”在40~50 ℃时反应可生成CuH。下列叙述中错误的是( )。
| A.“某物质”具有还原性 |
| B.CuH与盐酸反应可能产生H2 |
| C.CuH与足量稀硝酸反应:CuH+3H++NO3-=Cu2++NO↑+2H2O |
| D.CuH在氯气中燃烧:CuH+Cl2=CuCl+HCl |
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为 ( )。
| A.2 mol | B.1 mol | C.0.5 mol | D.0.25 mol |