题目内容
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯塑料得到的产物如下表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
碳
碳
;在试验中大试管管口倾斜向上的原因是塑料先熔化成液体,再分解
塑料先熔化成液体,再分解
.(2)试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有
4
4
种.(3)锥形瓶C中观察到的现象是
溴水褪色分层
溴水褪色分层
;经溴水充分吸收再干燥后,剩余两种气体的成份为氢气和甲烷
氢气和甲烷
,其平均相对分子质量为4.8
4.8
.分析:(1)根据最后最终残余物为固体;根据塑料加热时要熔化来分析;
(2)先找出能使酸性高锰酸钾溶液褪色的物质,再找出物质的一氯代物的种类;
(3)根据进入锥形瓶C的气体乙烯、丙烯能使溴水褪色分层,剩余气体为氢气、甲烷,根据摩尔质量在数值上等于相对分子质量,求出混合气体的平均相对分子质量.
(2)先找出能使酸性高锰酸钾溶液褪色的物质,再找出物质的一氯代物的种类;
(3)根据进入锥形瓶C的气体乙烯、丙烯能使溴水褪色分层,剩余气体为氢气、甲烷,根据摩尔质量在数值上等于相对分子质量,求出混合气体的平均相对分子质量.
解答:解:(1)因最后最终残余物为固体,所以为碳,因塑料加热是要熔化,所以在试验中大试管管口倾斜向上是为了让塑料先熔化成液体,再分解,
故答案为:碳; 塑料先熔化成液体,再分解;
(2)因试管B收集到的产品是苯和甲苯,甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色,所以甲苯的一氯代物有4种,故答案为:4;
(3)因乙烯、丙烯能使溴水褪色分层,经溴水充分吸收再干燥后,剩余两种气体的成份为氢气和甲烷,
设混合气体的质量为100g,则氢气的质量为12g,物质的两为6mol,甲烷的质量为24g,物质的量为1.5mol,
混合气体的摩尔质量为:
=4.8g/mol,即均相对分子质量为4.8,
故答案为:溴水褪色分层;4.8.
故答案为:碳; 塑料先熔化成液体,再分解;
(2)因试管B收集到的产品是苯和甲苯,甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色,所以甲苯的一氯代物有4种,故答案为:4;
(3)因乙烯、丙烯能使溴水褪色分层,经溴水充分吸收再干燥后,剩余两种气体的成份为氢气和甲烷,
设混合气体的质量为100g,则氢气的质量为12g,物质的两为6mol,甲烷的质量为24g,物质的量为1.5mol,
混合气体的摩尔质量为:
| 12g+24g |
| 6mol+1.5mol |
故答案为:溴水褪色分层;4.8.
点评:本题是一道实验综合题,知识点较多,难度不大,考查了学生分析问题的能力.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
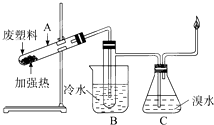 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图.加热聚丙烯废塑料得到的产物如下表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图.加热聚丙烯废塑料得到的产物如下表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
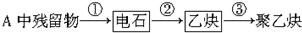
写出反应②③的化学方程式:
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有
(3)锥形瓶C中观察到的现象
(4)写出C中逸出的气体在工业上的两种用途:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。加热聚丙烯废塑料得到的产物如下表:

产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
质量分数/% | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
![]()
写出反应②的化学方程式_________________________。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有________种。
(3)锥形瓶C中观察到的现象__________________。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为__________。
(4)写出C中逸出的气体在工业上的两种用途_________、_________。
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。

加热聚丙烯废塑料得到的产物如下表:
产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
![]()
A中残留物①电石②乙炔③聚乙炔
写出反应②③的化学方程式_______________________________________________________、____________________________________________。
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有______种。
(3)锥形瓶C中观察到的现象______________________________。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为___________。
(4)写出C中逸出的气体在工业上的两种用途________、________。
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如表:

 、
、 、
、