题目内容
(13分)A、B、C、D、E、X、Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):
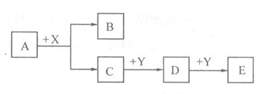
(1)若A为金属单质,B为氢气,X为盐酸,Y为易溶强碱溶液。则A物质的名称是 ;D与Y反应的离子方程式为;
(2)若A为固体非金属单质,B为水,X为强酸,Y为含钠元素的化合物。则A物质的名称可能是 ;D与Y反应的离子方程式为可能为
;
(3)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则D溶液显 (填酸或碱)性,原因是
(用离子方程式作答)
将NaOH溶液加入E的溶液中,可观察到的现象是 ;
D→E的化学反应方程式为 。

(1)若A为金属单质,B为氢气,X为盐酸,Y为易溶强碱溶液。则A物质的名称是 ;D与Y反应的离子方程式为;
(2)若A为固体非金属单质,B为水,X为强酸,Y为含钠元素的化合物。则A物质的名称可能是 ;D与Y反应的离子方程式为可能为
;
(3)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则D溶液显 (填酸或碱)性,原因是
(用离子方程式作答)
将NaOH溶液加入E的溶液中,可观察到的现象是 ;
D→E的化学反应方程式为 。
(1)铝;(1分) OH-+Al(OH)3=AlO2-↑+2H2O;(2分)(无↑扣1分)
(2) 碳或硫 ;(1分)
OH-+HCO3-=CO32-+H2O或OH-+HSO3-=SO32-+H2O;(2分)
(3) 酸 ;(1分) Fe3++3H2O Fe(OH)3↓+3H+(2分)(无↓扣1分)
Fe(OH)3↓+3H+(2分)(无↓扣1分)
先出现白色沉淀然后沉淀迅速变成灰绿色,最终变成红褐色;(2分)
2FeBr3+ Fe=3FeBr2 。(2分)
(2) 碳或硫 ;(1分)
OH-+HCO3-=CO32-+H2O或OH-+HSO3-=SO32-+H2O;(2分)
(3) 酸 ;(1分) Fe3++3H2O
 Fe(OH)3↓+3H+(2分)(无↓扣1分)
Fe(OH)3↓+3H+(2分)(无↓扣1分)先出现白色沉淀然后沉淀迅速变成灰绿色,最终变成红褐色;(2分)
2FeBr3+ Fe=3FeBr2 。(2分)
(1)根据图中的转化特点可知,C和强碱反应生成物D还能溶解在强碱中,常见的是铝的化合物的转化,再结合A是金属可知,A是铝和盐酸的÷生成氢气和氯化铝,所以D是氢氧化铝,E是偏铝酸钠。
(2)常见非金属单质能和酸反应生成水的,一般强氧化性酸和C或S反应,生成的CO2或SO2可与氢氧化钠反应生成正盐或酸式盐。
(3)常见的液体单质是溴,A能置换出溴,说明A是氯气。根据转化特点可判断,Y是变价的金属铁。铁离子在溶液中存在水解平衡,溶液显酸性。
(2)常见非金属单质能和酸反应生成水的,一般强氧化性酸和C或S反应,生成的CO2或SO2可与氢氧化钠反应生成正盐或酸式盐。
(3)常见的液体单质是溴,A能置换出溴,说明A是氯气。根据转化特点可判断,Y是变价的金属铁。铁离子在溶液中存在水解平衡,溶液显酸性。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
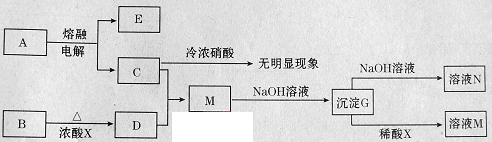
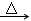 X+CO2↑+H2O
X+CO2↑+H2O X+O2
X+O2
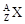 ,其氯化物化学式为XCl2,取该氯化物1.11g
,其氯化物化学式为XCl2,取该氯化物1.11g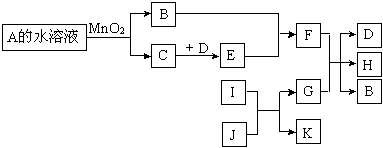
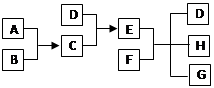
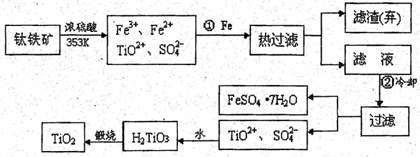
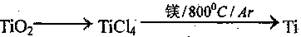
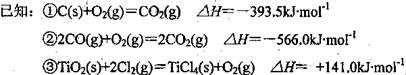
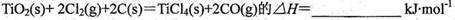
 在氩气氛中进行的理由是 。 (4)TiO2是白色粉末,不溶于水,也不溶于酸,但能溶于氢氟酸和热的浓硫酸中。请写出TiO2与浓硫酸反应的化学方程式 。
在氩气氛中进行的理由是 。 (4)TiO2是白色粉末,不溶于水,也不溶于酸,但能溶于氢氟酸和热的浓硫酸中。请写出TiO2与浓硫酸反应的化学方程式 。