��Ŀ����
�跴Ӧ��Fe(s)+CO2(g) FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1��
��Ӧ��Fe(s)+H2O(g) FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
��1�����ϱ����ƶϣ���Ӧ����________(��š�������)�ȷ�Ӧ��
��2�����з�Ӧ��H2(g)+CO2(g) CO(g)+H2O(g)��H=Q3
CO(g)+H2O(g)��H=Q3
�ٸ��ݷ�Ӧ������Ƶ���K1��K2��K3�Ĺ�ϵʽK3=_____________�����ƶϷ�Ӧ����________(��š�������)�ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________��
A����С������� B�������¶� C��ʹ�ú��ʵĴ���
D���跨����CO����E�������¶�
�ڸ��ݷ�Ӧ������Ƶ���Q1��Q2��Q3�Ĺ�ϵʽQ3=_____________��
 FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1����Ӧ��Fe(s)+H2O(g)
 FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�| �¶�(T) | K1 | K2 |
| 973 | 1��47 | 2��38 |
| 1173 | 2��15 | 1��67 |
��1�����ϱ����ƶϣ���Ӧ����________(��š�������)�ȷ�Ӧ��
��2�����з�Ӧ��H2(g)+CO2(g)
 CO(g)+H2O(g)��H=Q3
CO(g)+H2O(g)��H=Q3�ٸ��ݷ�Ӧ������Ƶ���K1��K2��K3�Ĺ�ϵʽK3=_____________�����ƶϷ�Ӧ����________(��š�������)�ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________��
A����С������� B�������¶� C��ʹ�ú��ʵĴ���
D���跨����CO����E�������¶�
�ڸ��ݷ�Ӧ������Ƶ���Q1��Q2��Q3�Ĺ�ϵʽQ3=_____________��
��1������
��2����K3=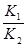 ��DE��Q3=Q1�DQ2
��DE��Q3=Q1�DQ2
��2����K3=
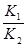 ��DE��Q3=Q1�DQ2
��DE��Q3=Q1�DQ2���������
��1�����ڷ�Ӧ����˵�������¶���ƽ�ⳣ������˵��ƽ�������ƶ�������ƽ���ƶ�ԭ��������ı�Ӱ�컯ѧƽ���һ����������ôƽ��������ܹ��������ָı�ķ����ƶ�����֪�����������ȵķ���
��2����Ӧ�ټ�ȥ��Ӧ�ھͿ��Եõ���Ӧ�ۣ�H2(g)+CO2(g)
 CO(g)+H2O(g)��H=Q3����˷�ӦӦ�۵�K3=
CO(g)+H2O(g)��H=Q3����˷�ӦӦ�۵�K3=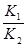 ���ӱ��е����ݿ�֪�������¶ȵ����ߣ�K3��ֵ�������ߵģ���˸÷�Ӧ�����ȷ�Ӧ����С���������ƽ�ⲻ�ƶ��������¶ȣ�ƽ�������ƶ���ʹ�ú��ʵĴ�����ƽ�ⲻ�ƶ����跨����CO��������С���������Ũ�ȣ�ƽ�����ƣ������¶ȣ�ƽ���������ȵķ����ƶ������ѡDE��Q3=Q1�DQ2
���ӱ��е����ݿ�֪�������¶ȵ����ߣ�K3��ֵ�������ߵģ���˸÷�Ӧ�����ȷ�Ӧ����С���������ƽ�ⲻ�ƶ��������¶ȣ�ƽ�������ƶ���ʹ�ú��ʵĴ�����ƽ�ⲻ�ƶ����跨����CO��������С���������Ũ�ȣ�ƽ�����ƣ������¶ȣ�ƽ���������ȵķ����ƶ������ѡDE��Q3=Q1�DQ2
��ϰ��ϵ�д�
�����Ŀ
 2SO3 (g)����H����197 kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��) 2 mol SO2��1 mol O2��(��) 1 mol SO2��0.5 mol O2��(��) 2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����
2SO3 (g)����H����197 kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��) 2 mol SO2��1 mol O2��(��) 1 mol SO2��0.5 mol O2��(��) 2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����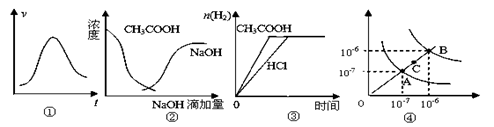
 B(g) + C(g)����H = ?48��25 kJ/L
B(g) + C(g)����H = ?48��25 kJ/L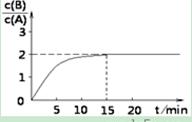
 2NO(g)��O2(g)��H>0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���
2NO(g)��O2(g)��H>0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���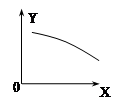
 2NO2��H>0���ܱ������з�Ӧ���ﵽƽ��״̬��Ҫʹ���������ɫ����ɲ�ȡ�ķ����� �ټ�Сѹǿ ����С����������¶Ȣ�����N2O4��Ũ�� �� ��
2NO2��H>0���ܱ������з�Ӧ���ﵽƽ��״̬��Ҫʹ���������ɫ����ɲ�ȡ�ķ����� �ټ�Сѹǿ ����С����������¶Ȣ�����N2O4��Ũ�� �� ��  2R(g) ��H��0����ͼ��Y����ָ
2R(g) ��H��0����ͼ��Y����ָ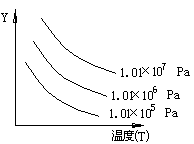
 2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����
2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����