题目内容
【题目】常温下,Ka(CH3COOH)=1.8×10-5,分别向20mL0.1mol/LNaHCO3溶液和CH3COOH溶液中逐滴加入0.1mol/LNaOH溶液,滴定曲线如图所示,下列叙述正确的是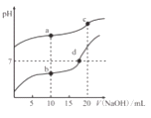
A. a点溶液中存在:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
B. b、d点溶液中离子浓度的大小关系均为c(Na+)3COO-)
C. C点溶液中存在:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
D. d点溶液中: n(CH3COO-)/n(CH3COOH)=180
【答案】D
【解析】NaHCO3溶液显碱性,CH3COOH溶液显酸性,因此曲线ac为NaHCO3溶液与NaOH的反应,bd为CH3COOH溶液与NaOH反应的曲线。A. a点溶液中的溶质为等物质的量的Na2CO3和NaHCO3,根据电荷守恒,存在:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故A错误;B. b点溶液显酸性,根据电荷守恒,c(Na+)<c(CH3COO-),d点溶液pH=7,根据电荷守恒,c(Na+)=c(CH3COO-),故B错误;C. C点溶液中的溶质为Na2CO3,根据质子守恒,存在:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-),故C错误;D. d点溶液的pH=7,Ka(CH3COOH)=  =1.8×10-5,则
=1.8×10-5,则 =
=![]() =180,故D正确;故选D。
=180,故D正确;故选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目