��Ŀ����
����Ŀ�����Ų��Ͽ�ѧ�ķ�չ�����������仯����õ���Խ��Խ�㷺��Ӧ�ã�������Ϊ���Ͻ�ά���ء�����֪����ԭ������Ϊ23���ش��������⣺
��1��������Ϊ��һ��ϡ��Ԫ�أ��㷺��ɢ�ڸ��ֿ����У��ط��˿��еķ�ԭ��������Ѵﵽ8 �����ȶ��ṹ���仯ѧʽΪK2H6U2V2O15�����з�Ԫ�صĻ��ϼ�Ϊ+5�ۣ����������������ʽ��ʾ���û�����Ļ�ѧʽΪ��_______________________________��
��2�������������ǹ�ҵ�����еij��ô������繤ҵ�������о������������������������Ӻ����ϴ����л��շ�����ͳ�ļ����ǡ��������շ���,���������Ϊ��
![]()
���б����ǽ�ʳ�κͷ�Ǧ���ڿ����б��գ���ʱ��ʯ��������V2O5��ת��ΪNaVO3��Ȼ����ˮ���ս���н���NaVO3������ϡ�����ữ�͵õ�V2O5��ˮ����������վͿɵõ�V2O5��
�������ڱ���ǰĥ���Ŀ����_______________________��
��д�����չ�����V2O5������Ӧ�Ļ�ѧ����ʽ��___________________________��
��3���ⶨ�������ķ������Ȱѷ�ת����V2O5��V2O5��������Һ��ת���VO���������ᡢ��������������Ȳⶨ������Ӧ�Ļ�ѧ����ʽΪ��VO2++H2C2O4==VO++2CO2+H2O������Ӧ����0.9 g ���ᣬ�μӷ�Ӧ�ķ�Ԫ��������_____g��
��4����V2O5Ϊ������ʹSO2ת��ΪSO3�ķ�Ӧ���£�2SO2(g)+O2(g)![]() 2SO3(g)��ij�¶��£�SO2��ƽ��ת����(a)����ϵ��ѹǿ(P)�Ĺ�ϵ��ͼ��ʾ��
2SO3(g)��ij�¶��£�SO2��ƽ��ת����(a)����ϵ��ѹǿ(P)�Ĺ�ϵ��ͼ��ʾ��

����ͼʾ�ش��������⣺
����2.0molSO2��1.0molO2����10L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10MPa���÷�Ӧ��ƽ�ⳣ������ʽΪ__________������______________��
��ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K��A��______K��B�������������������=������
���𰸡� K2O��V2O5��2UO3�� 3H2O ����Ӵ������ʹ��Ӧ��ֽ��� 2V2O5+4NaCl+O2![]() 4NaVO3+ 2Cl2 0.51 K=
4NaVO3+ 2Cl2 0.51 K=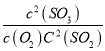 800L��mol-1 =
800L��mol-1 =
��������(1) �����������ʽ��ʾ��ǰ���DZ��ָ���Ԫ�ػ��ϼ۲��䣬���Կ�ͬʱ��ԭ�Ӹ���������ͬ�ı���������ѧʽ��K2O��V2O5��2UO3��3H2O����2���ٷ����Ŀ��������Ӵ��������߷�Ӧ���ʣ�ʹ��Ӧ���ַ�Ӧ���ڸ��ݵ��ӵĵ�ʧ�غ��֪�����չ�����V2O5������Ӧ�Ļ�ѧ����ʽԭ��2V2O5+4NaCl+O2![]() 4NaVO3+ 2Cl2��(3)0.9g��������ʵ�����
4NaVO3+ 2Cl2��(3)0.9g��������ʵ�����![]() ��0.01mol������ݷ�Ӧ�Ļ�ѧ����ʽVO2++H2C2O4==VO++2CO2+H2O��֪���μӷ�Ӧ�ķ�Ԫ�ص�������0.01mol��51g/mol��0.51g����4���ٷ�Ӧ2SO2(g)+O2(g)
��0.01mol������ݷ�Ӧ�Ļ�ѧ����ʽVO2++H2C2O4==VO++2CO2+H2O��֪���μӷ�Ӧ�ķ�Ԫ�ص�������0.01mol��51g/mol��0.51g����4���ٷ�Ӧ2SO2(g)+O2(g)![]() 2SO3(g)��ƽ�ⳣ������ʽΪK=
2SO3(g)��ƽ�ⳣ������ʽΪK= ��
��
2SO2(g) �� O2(g) ![]() 2SO3(g)
2SO3(g)
��ʼ 2 1 0
ת�� 1.6 0.8 1.6
ƽ�� 0.4 0.2 1.6
K= =800 L��mol-1��
=800 L��mol-1��
��ƽ�ⳣ�����¶ȱ仯��ƽ��״̬��A�䵽Bʱ���¶Ȳ��䣬ƽ�ⳣ�����䣬��K��A��=K��B����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�





