题目内容
【题目】用下图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
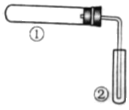
①中实验 | ②中现象 | |
A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
【答案】A
【解析】
试题A.试管中空气也能使肥皂水冒泡;
B.氯化铵和氢氧化钙混合加热生成氨气,氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而使溶液呈红色;
C.二氧化碳能使澄清石灰水变浑浊;
D.不饱和烃能使溴的四氯化碳褪色.
解:A.加热过程中的热空气、铁和水蒸气反应生成的氢气都能使肥皂水冒泡,所以肥皂水冒泡该反应不一定发生,故A错误;
B.NH4Cl+Ca(OH)2![]() NH3↑+CaCl2+H2O、NH3+H2ONH3.H2ONH4++OH﹣,氨水溶液呈碱性,所以能使酚酞试液变红色,故B正确;
NH3↑+CaCl2+H2O、NH3+H2ONH3.H2ONH4++OH﹣,氨水溶液呈碱性,所以能使酚酞试液变红色,故B正确;
C.2NaHCO3![]() Na2CO3+CO2↑+H2O,二氧化碳能使澄清石灰水变浑浊,如果②中澄清石灰水变浑浊,则①中一定发生反应,故C正确;
Na2CO3+CO2↑+H2O,二氧化碳能使澄清石灰水变浑浊,如果②中澄清石灰水变浑浊,则①中一定发生反应,故C正确;
D.溴的四氯化碳褪色说明有不饱和烃生成,所以①中一定发生化学反应,故D正确;
故选A.

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】工业废水中常含有一定量氧化性较强的Cr2O72-,利用滴定原理测定Cr2O72-含量方法如下:
步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液充分反应:Cr2O72-+6I-+14H+ === 2Cr3++3I2+7H2O。
步骤Ⅲ:向锥形瓶中滴入几滴指示剂。用滴定管量取0.1000 molL-1Na2S2O3溶液进行滴定,数据记录如下:(I2+2Na2S2O3 === 2NaI+Na2S4O6)
滴定次数 | Na2S2O3溶液起始读数/mL | Na2S2O3溶液终点读数/mL |
笫一次 | 1.02 | 19.03 |
第二次 | 2.00 | 19.99 |
第三次 | 0. 20 | a |
(1)步骤Ⅰ量取30.00 mL废水选择的仪器是_____。
(2)步骤Ⅲ中滴加的指示剂为_____。滴定达到终点的实验现象是____。
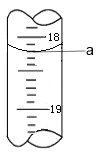
(3)步骤Ⅲ中a 的读数如图所示,则:
① a=_____。
② Cr2O72-的含量为____gL-1。
(4)以下操作会造成废水中Cr2O72-含量测定值偏高的是_____。
A. 滴定终点读数时,俯视滴定管的刻度
B. 盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D. 量取Na2S2O3溶液的滴定管用蒸馏水洗后未用标准液润洗
【题目】下列各组物质中,X既能与Y反应又能与Z反应的是
Y | X | Z | |
① | H2O(g) | Fe | ZnSO4溶液 |
② | KOH溶液 | Al | 稀硫酸 |
③ | Si | Cl2 | H2 |
④ | 酸性高锰酸钾溶液 | Fe2+(aq) | 漂白液 |
A.①③B.①④C.②③④D.②③