题目内容
用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )A.14g氮气中含有7NA个电子
B.1molCl2作为氧化剂得到的电子数为NA
C.通常状况下,NA个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-数为NA
【答案】分析:1mol氮气中含有14NA个电子;Cl2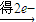 2Cl-;标准状况下,NA个CO2分子占有的体积才为22.4L;0.5moMgCl2含有Cl-数为NA.
2Cl-;标准状况下,NA个CO2分子占有的体积才为22.4L;0.5moMgCl2含有Cl-数为NA.
解答:解:A、1mol氮气中含有14NA个电子,0.5mol氮气中含有7NA个电子,故A正确;
B、Cl2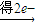 2Cl-,1molCl2作为氧化剂得到的电子数为2NA,故B错误;
2Cl-,1molCl2作为氧化剂得到的电子数为2NA,故B错误;
C、在标准状况下,NA个CO2分子占有的体积才为22.4L,故C错误;
D、题目中没说MgCl2溶液的体积是1L,即溶液的体积不确定,则氯离子的数目不确定,故D错误;
故选A.
点评:本题考查阿伏伽德罗常数的计算,明确物质中的电子数、氧化还原反应中的电子数的计算即可解答,并注意状况来分析,学生易错选D.
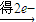 2Cl-;标准状况下,NA个CO2分子占有的体积才为22.4L;0.5moMgCl2含有Cl-数为NA.
2Cl-;标准状况下,NA个CO2分子占有的体积才为22.4L;0.5moMgCl2含有Cl-数为NA.解答:解:A、1mol氮气中含有14NA个电子,0.5mol氮气中含有7NA个电子,故A正确;
B、Cl2
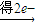 2Cl-,1molCl2作为氧化剂得到的电子数为2NA,故B错误;
2Cl-,1molCl2作为氧化剂得到的电子数为2NA,故B错误;C、在标准状况下,NA个CO2分子占有的体积才为22.4L,故C错误;
D、题目中没说MgCl2溶液的体积是1L,即溶液的体积不确定,则氯离子的数目不确定,故D错误;
故选A.
点评:本题考查阿伏伽德罗常数的计算,明确物质中的电子数、氧化还原反应中的电子数的计算即可解答,并注意状况来分析,学生易错选D.

练习册系列答案
相关题目