题目内容
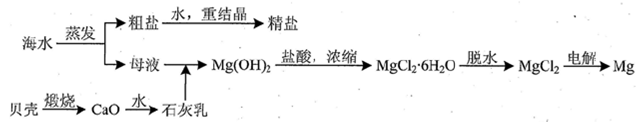
从海水中提取镁的工业生产流程如下:

下列说法错误的是

下列说法错误的是
| A.此法的优点之一是原料来源丰富 |
| B.该提取镁的过程中涉及置换、分解、复分解和氧化还原反应 |
| C.步骤①②③的目的是从海水中提取无水MgCl2 |
| D.步骤②中加盐酸的离子方程式为Mg(OH)2+2H+=Mg2++2H2O |
B
试题分析:CaCO3
 CaO+CO2,CaO+H2O=Ca(OH)2, Ca(OH)2+MgCl2= CaCl2+Mg(OH)2↓, Mg(OH)2+2HCl= 2H2O +MgCl2, MgCl2
CaO+CO2,CaO+H2O=Ca(OH)2, Ca(OH)2+MgCl2= CaCl2+Mg(OH)2↓, Mg(OH)2+2HCl= 2H2O +MgCl2, MgCl2 Mg+Cl2↑. A.此法的优点之一是原料贝壳、海水来源丰富。正确。B.该提取镁的过程中并未涉及置换反应,错误。 C.步骤①②③的目的是从海水中提取无水MgCl2,正确。 D.步骤②中加盐酸的离子方程式为Mg(OH)2+2H+=Mg2++2H2O,正确。
Mg+Cl2↑. A.此法的优点之一是原料贝壳、海水来源丰富。正确。B.该提取镁的过程中并未涉及置换反应,错误。 C.步骤①②③的目的是从海水中提取无水MgCl2,正确。 D.步骤②中加盐酸的离子方程式为Mg(OH)2+2H+=Mg2++2H2O,正确。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目