题目内容
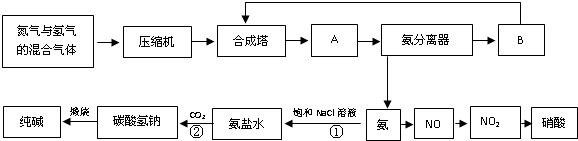
有关合成氨工业的说法中,正确的是( )
分析:A、虽然反应出来的混合气体中NH3比较低,但原料循环使用,连续化生产,所以生产氨的工厂效率不低.
B、由于氨易液化,可以抽出氨气,使平衡正移,提高原料转化率,而且N2、H2是循环使用;
C、合成氨是放热反应,所以低温有利,但反应速率跟温度有关,温度越高速率越大;
D、反应是分子数减小的反应,高压有利于向正反应移动.
B、由于氨易液化,可以抽出氨气,使平衡正移,提高原料转化率,而且N2、H2是循环使用;
C、合成氨是放热反应,所以低温有利,但反应速率跟温度有关,温度越高速率越大;
D、反应是分子数减小的反应,高压有利于向正反应移动.
解答:解:A、虽然反应出来的混合气体NH3比较低,但原料循环使用,连续化生产,所以生产氨的工厂效率不低,故A错误.
B、由于氨易液化,可以抽出氨气,使平衡正移,提高原料转化率,而且N2、H2是循环使用,所以总体来说氨的生产率很高,故B正确;
C、合成氨是放热反应,所以低温有利,但反应速率跟温度有关,温度越高速率越大,所以温度是取在既保证一定速率,又保证反应尽量向正反应移动,同时还要确保催化剂活性,因为催化剂活性跟温度关系极大.一般合成氨反应500℃是保证催化活性最大,不是为了使化学平衡向正反应方向移动,故C错误.
D、合成氨的反应是分子数减小的反应,高压有利于向正反应方向移动,且能提高正反应速率,跟催化剂无关,故D错误;
故选B.
B、由于氨易液化,可以抽出氨气,使平衡正移,提高原料转化率,而且N2、H2是循环使用,所以总体来说氨的生产率很高,故B正确;
C、合成氨是放热反应,所以低温有利,但反应速率跟温度有关,温度越高速率越大,所以温度是取在既保证一定速率,又保证反应尽量向正反应移动,同时还要确保催化剂活性,因为催化剂活性跟温度关系极大.一般合成氨反应500℃是保证催化活性最大,不是为了使化学平衡向正反应方向移动,故C错误.
D、合成氨的反应是分子数减小的反应,高压有利于向正反应方向移动,且能提高正反应速率,跟催化剂无关,故D错误;
故选B.
点评:本题考查了合成氨的原理,同时考查了外界条件对化学平衡的影响,比较基础,注意理解温度、浓度、压强、催化剂等外界条件对化学平衡的影响.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化
步骤及生成物未列出):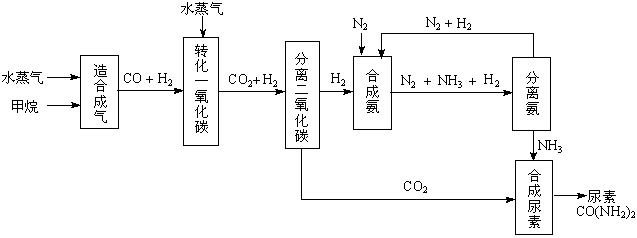
(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)  CO(g)+3H2(g);△H>0在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是 。
CO(g)+3H2(g);△H>0在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是 。
A、增大压强 B、升高温度 C、充入He气 D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g) +CO(g) 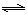 H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(3)有关合成氨工业的说法中正确的是 。
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3)∶n(CO2)的最佳配比为 ,而实际生产过程中,往往使n(NH3)∶n(CO2)≥3,这是因为 。
(5)当甲烷合成氨气的转化率为60%时,以3.0×108 L甲烷为原料能够合成 L 氨气。(假设体积均在标准状况下测定)