题目内容
下列物质加入水中显著放热的是( )。
| A.生石灰 | B.固体NaCl | C.无水乙醇 | D.固体NH4NO3 |
A
解析

氯原子对O3分解有催化作用:O3+Cl=ClO+O2 ΔH1,ClO+O=Cl+O2 ΔH2,大气臭氧层的分解反应是:O3+O=2O2 ΔH,该反应的能量变化示意图如图所示,下列叙述中,正确的是( )
| A.反应O3+O=2O2的ΔH=E1-E3 |
| B.反应O3+O=2O2的ΔH=E2-E3 |
| C.O3+O=2O2是吸热反应 |
| D.ΔH=ΔH1+ΔH2 |
甲烷是一种高效清洁的新能源,0.25 mol CH4完全燃烧生成液态水时放出222.5 kJ热量,则下列热化学方程式中正确的是( )
A.2CH4(g)+4O2(g) 2CO2(g)+4H2O(l) ΔH="+890" kJ·mol-1 2CO2(g)+4H2O(l) ΔH="+890" kJ·mol-1 |
B.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="+890" kJ·mol-1 CO2(g)+2H2O(l) ΔH="+890" kJ·mol-1 |
C.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="-890" kJ·mol-1 CO2(g)+2H2O(l) ΔH="-890" kJ·mol-1 |
D.2CH4(g)+4O2(g) 2CO2(g)+4H2O(l) ΔH="-890" kJ·mol-1 2CO2(g)+4H2O(l) ΔH="-890" kJ·mol-1 |
在反应键的H2+Cl2=2HCl中,已知H—H键的键能为436 kJ·mol-1,Cl—Cl键的键能为243 kJ·mol-1,H—Cl键的键能为431 kJ·mol-1,判断当1 mol H2与1 mol Cl2反应生成2 mol HCl时该反应( )。
| A.是吸热反应 |
| B.是放热反应 |
| C.吸收183 kJ热量 |
| D.放出183 kJ热量 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是( )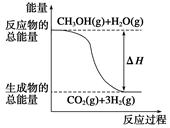
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+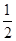 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
下列说法正确的是( )
| A.CH3OH的燃烧热为192.9 kJ·mol-1 |
| B.反应①中的能量变化如图所示 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
D.根据②推知反应:CH3OH(l)+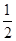 O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 |
已知反应H2(g)+Br2(l)=2HBr(g)在25 ℃、101 kPa下进行,放出热量为72 kJ,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
| | H2(g) | Br2(g) | HBr(g) |
| 1 mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为( )。
A.404 B.260 C.230 D.200
已知断开或形成1 mol化学键吸收或放出的能量称为化学键的键能,如H—H键的键能为436 kJ·mol-1,N≡N键的键能为945 kJ·mol-1,N—H键的键能为391 kJ·mol-1。则下列有关工业合成氨反应的热化学方程式正确的是 ( )
A.N2(g)+3H2(g)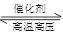 2NH3(g) ΔH=-93 kJ·mol-1 2NH3(g) ΔH=-93 kJ·mol-1 |
B.N2(g)+3H2(g)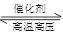 2NH3(g) ΔH=+1471 kJ·mol-1 2NH3(g) ΔH=+1471 kJ·mol-1 |
C.N2(g)+3H2(g)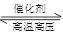 2NH3(g) ΔH=+93 kJ·mol-1 2NH3(g) ΔH=+93 kJ·mol-1 |
D.N2(g)+3H2(g)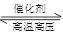 2NH3(g) ΔH=-1471 kJ·mol-1 2NH3(g) ΔH=-1471 kJ·mol-1 |
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) ΔH1
2H2(g)+O2(g)=2H2O(g) ΔH2
C(s)+O2(g)=CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为( )。
| A.12ΔH3+5ΔH2-2ΔH1 | B.2ΔH1-5ΔH2-12ΔH3 |
| C.12ΔH3-5ΔH2-2ΔH1 | D.ΔH1-5ΔH2-12ΔH3 |
化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )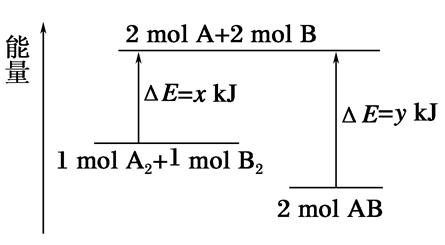
| A.该反应是吸热反应 |
| B.断裂1mol A—A键和1mol B—B键能放出xkJ的能量 |
| C.断裂2mol A—B键需要吸收ykJ的能量 |
| D.2mol AB的总能量高于1 mol A2和1mol B2的总能量 |