题目内容
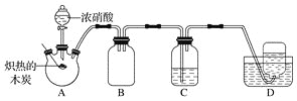
【题目】下列操作或叙述正确的是![]()
![]()
A.配制![]() 溶液时,将溶解后的NaOH溶液立即注入容量瓶
溶液时,将溶解后的NaOH溶液立即注入容量瓶
B.用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶
C.向某溶液中加入![]() 溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有SO42-
溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有SO42-
D.向沸水中逐滴滴加![]() 溶液,并不断用玻璃棒搅拌,可制得
溶液,并不断用玻璃棒搅拌,可制得![]() 胶体
胶体
【答案】B
【解析】
A.配制![]() 溶液时,溶解后的NaOH溶液应冷却至室温,才能注入容量瓶,故A错误;
溶液时,溶解后的NaOH溶液应冷却至室温,才能注入容量瓶,故A错误;
B.实验中剩余的液体药品和粉末状药品不能放回原试剂瓶,但是块状的药品可以放回原试剂瓶,故B正确;
C.向某溶液中加入氯化钡溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中含有硫酸根离子或银离子,故C错误;
D.用玻璃棒搅拌胶体,会引起胶体的聚沉,故D错误;
故答案为B。

【题目】阅读下面的信息,推断元素及有关物质,按要求回答物质:
信息①:X、Y、Z、W是常见的短周期元素,其原子序数依次增大,且原子核外最外层电子数均不少于2。
(1)根据信息①:X一定不是_________(填序号).
A.氢 | B.碳 | C.氧 | D.硫 |
信息②:上述四种元素的单质均能在足量的氧气中燃烧,生成的四种氧化物中,有两种能溶
于稀硫酸,三种能溶于浓氢氧化钠溶液,氧化物的相对分子质量都大于26。
(2)这四种元素中是否可能有一种是铝元素?_____________________________________。
信息③:向上述四种元素单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤,向
滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀。
(3)白色沉淀物的化学式为____________________________________________________。
信息④:向上述四种元素单质组成的混合物中加入足量烧碱溶液,固体部分溶解,过滤,向
滤液中加入过量的盐酸溶液,最终溶液中析出白色沉淀。
(4)生成白色沉淀物的离子方程式为____________________________________________。
信息⑤:X与W同主族
(5)X与浓硫酸加热时反应的化学方程式为_______________________________________。