题目内容
(2010?西城区模拟)25℃时,下列各溶液中关系的叙述中,正确的是( )
分析:A.pH越小,c(H+)越大;
B.从溶液满足电荷守恒的角度分析;
C.溶液应呈碱性;
D.pH相同的盐溶液中,对应的酸越弱,水解程度越大,溶液浓度越小.
B.从溶液满足电荷守恒的角度分析;
C.溶液应呈碱性;
D.pH相同的盐溶液中,对应的酸越弱,水解程度越大,溶液浓度越小.
解答:解:A.pH=2的盐酸中c(H+)=0.01mol/L,pH=l的硫酸溶液中c(H+)=0.1mol/L,二者之比为1:10,故A错误;
B.任何溶液都满足电荷守恒,该溶液中存在c(Na+)+c(H+)═c(OH-)+c(CH3COO-),故B正确;
C.BA为强碱弱酸盐,溶液呈碱性,pH>7,故C错误;
D.酸性:CH3COOH>H2CO3>C6H5OH,pH相同的盐溶液中,对应的酸越弱,水解程度越大,溶液浓度越小,c(Na+)的大小顺序是①>③>②,NaOH为强碱,c(Na+)最小,正确顺序为①>③>②>④,故D错误.
故选B.
B.任何溶液都满足电荷守恒,该溶液中存在c(Na+)+c(H+)═c(OH-)+c(CH3COO-),故B正确;
C.BA为强碱弱酸盐,溶液呈碱性,pH>7,故C错误;
D.酸性:CH3COOH>H2CO3>C6H5OH,pH相同的盐溶液中,对应的酸越弱,水解程度越大,溶液浓度越小,c(Na+)的大小顺序是①>③>②,NaOH为强碱,c(Na+)最小,正确顺序为①>③>②>④,故D错误.
故选B.
点评:本题考查离子浓度的大小比较,题目难度中等,易错点为D,注意盐类水解程度的比较.

练习册系列答案
相关题目
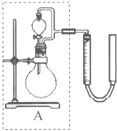 (2010?西城区一模)过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.
(2010?西城区一模)过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.